Polymer afledt af materiale i rejeskaller kunne levere anti-cancermedicin til tumorsteder
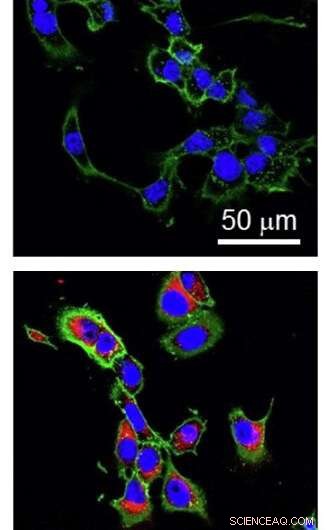
Disse billeder viser brystkræftceller fra mus taget under et mikroskop. På begge billeder grøn angiver cellemembranen, og blå angiver kernen. Celler i det nederste billede er blevet behandlet med Taxol-ladede nanopartikler, mens cellerne i det øverste billede ikke har. Den røde farve indikerer tilstedeværelsen af nanopartikler inde i cellerne. Skalaen er 50 mikrometer. Kredit:Mu et al., Materialer i dag, 2020
Lægemiddellevering er en tilbagevendende gåde i kræftbehandling. Forskere har udviklet mange anti-cancer terapeutiske midler. Men disse stoffer skader ofte sundt væv, og lægemidler kan endda nedbrydes i blodbanen, før de når tumorstedet. Lægemidler mod kræft kan holde længere, hvis de opløses i visse kemiske opløsninger, men mange kommer med potentielt giftige bivirkninger.
Nanopartikler er en lovende type lægemiddelleveringssystem. Også kendt som nanobærere, disse små partikler kan binde sig til lægemidler og beskytte dem mod nedbrydning, indtil de trænger ind i tumorceller. Men deres effektivitet som lægemiddelbærere og lægemiddelbeskyttere, samt potentiel toksicitet hos patienter, afhænger meget af deres størrelse, sammensætning og kemiske egenskaber. At balancere disse konkurrerende faktorer er en delikat proces. Selvom forskere har gjort betydelige fremskridt inden for nanomedicin i det sidste årti, det forblev en formidabel udfordring at designe og syntetisere små, stabile nanopartikler, der kunne levere tilstrækkelig medicin til at behandle solide tumorer.
Tidligere i år meddelte forskere ved University of Washington, at de har opnået en sådan balancegang med et nanopartikelbaseret lægemiddelleveringssystem, der sikkert kan transportere et potent anti-cancerlægemiddel gennem blodbanen. Som de rapporterer i et papir offentliggjort i maj i Materialer i dag , deres nanopartikel er afledt af kitin, en naturlig og organisk polymer, der, blandt andet, udgør de ydre skaller af rejer.
Holdet, ledet af Miqin Zhang, en UW professor i materialevidenskab og teknik og i neurologisk kirurgi, demonstreret, at deres kitin-afledte system med succes kan transportere Taxol, et potent lægemiddel mod kræft, der også er kendt som paclitaxel, gennem blodbanen og hæmmer tumorvækst og spredning, også kendt som metastase, hos mus. Nanopartiklerne viste ingen negative bivirkninger, sandsynligvis, da de til dels stammer fra naturligt forekommende polymer.
"Dette kunne danne grundlaget for en ny klasse af nanopartikelleveringssystemer, der kan transportere anti-cancer-terapi gennem kroppen sikkert, uden giftige bivirkninger fra nanopartikelmaterialet, " sagde Zhang, som også er fakultetsforsker ved UW Institute for Nano-Engineered Systems og Molecular Engineering and Sciences Institute.
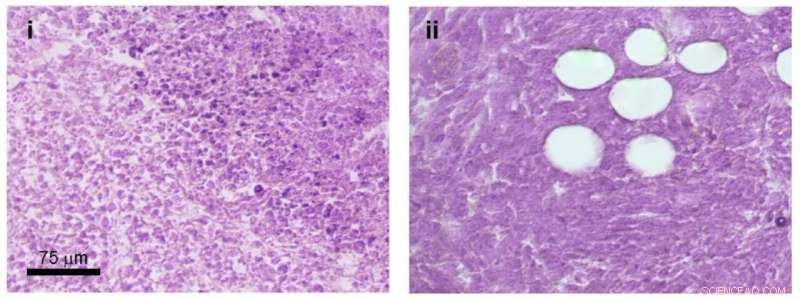
Disse billeder viser vævsprøver taget fra muse brysttumorer. Billedet til venstre er fra en svulst, der ikke har modtaget noget kræftlægemiddel. Billedet til højre er fra en tumor behandlet med Taxol-ladede nanopartikler. Celler til højre er unormalt formet og er adskilt af hvide "boblede" områder, som ses i musetumorer behandlet med Taxol. Skalaen er 75 mikrometer. Kredit:Mu et al., Materialer i dag , 2020
Nanopartiklerne, en gang fyldt med Taxol, er omkring 20,6 nanometer i diameter. Det er omkring 1/4000 af bredden af et menneskehår, ifølge U.S. National Nanotechnology Initiative. Partiklerne er små nok til at rejse gennem blodkar og komme til potentielt kompakte tumorsteder.
Zhangs team startede med at lade Taxol-partikler på meget længere strenge af chitosan, et materiale afledt af kitin. Nanofibrene nedbrydes og danner nanopartikler, når de udsættes for serum, et blodprotein, enten i laboratoriet eller i kroppen. Forskere viste, at lægemiddelfyldte nanofibre, når det injiceres i mus, brød hurtigt ned i de små nanopartikler - takket være serumproteiner i blodet - og kunne cirkulere frit i blodbanen, komme ind i organer og nå tumorsteder.
Holdet udsatte Taxol-ladede nanopartikler for en byge af eksperimenter for at se, hvad de kunne gøre ved tumorer. I cellekulturer af muse brystkræftceller, et flertal af kræftceller viste tegn på celledød 48 timer efter behandling, hvilket indikerer, at nanopartikel-associeret Taxol kunne trænge ind i kræftceller og forringe cellevækst mindst lige så godt som fritflydende Taxol. Hos mus, Taxol-fyldte nanofibre, som brød ned til nanopartikler, viste 90 % hæmning af brysttumorvækst sammenlignet med ca. 66 % hæmning for Taxol injiceret i den kliniske opløsning, der anvendes i vid udstrækning i dag. Nanopartiklerne hæmmede også melanom tumorvækst hos mus med op til 75 %. I separate forsøg med mus, Taxolfyldte nanopartikler forhindrede også spredning af brystkræft til andre dele af kroppen, i modsætning til Taxol i en klinisk løsning.
Ud over disse lovende fund med tumorer, holdet fandt ud af, at nanopartiklerne holdt Taxol cirkulerende i blodbanen længere, give lægemidlet mere tid til at nå tumorstedet. I blodbanen hos mus, halveringstiden for Taxol-associerede nanopartikler var næsten 25 timer, sammenlignet med mindre end 2 timer for Taxol injiceret i den kliniske opløsning. Mus injiceret med nanofibrene viste ingen tegn på toksiske bivirkninger, hvilket indikerer, at nanopartiklerne i sig selv ikke forårsagede skade på væv. I modsætning, den kliniske opløsning, der anvendes i vid udstrækning i dag til Taxol, kan forårsage levertoksicitet hos mus, blandt andre bivirkninger.
Zhang mener, at de chitosan-afledte nanopartikler kunne danne grundlaget for et ikke-toksisk lægemiddelleveringssystem for kræft, der holder terapeutika i kroppen længere for at hæmme tumorvækst og metastaser.
"Dette er en meget lovende opdagelse. Mange lægemiddelleveringssystemer, der bruges i dag til anti-cancermedicin, kommer med toksiske bivirkninger, og ikke beskytte lægemidlet i særlig lang tid i patientens krop, " sagde Zhang. "Nanopartiklerne har alle de egenskaber, du kunne håbe på, for at få stoffet ind i tumorceller. Den lille chitosan-baserede nanobærer, lavet på stedet, med unik biokompatibilitet og bionedbrydelighed, tilbyder en ny strategi for anti-cancer medicin levering og har et stort potentiale for hurtig oversættelse til klinikken."
 Varme artikler
Varme artikler
-
 Meget følsom dopamindetektor bruger 2-D materialerSkematisk af en meget selektiv dopamindetektor ved brug af todimensionelt materiale. Kredit:Derrick Butler, Penn State En superfølsom dopamindetektor kan hjælpe med tidlig diagnosticering af flere
Meget følsom dopamindetektor bruger 2-D materialerSkematisk af en meget selektiv dopamindetektor ved brug af todimensionelt materiale. Kredit:Derrick Butler, Penn State En superfølsom dopamindetektor kan hjælpe med tidlig diagnosticering af flere -
 Hvad er ulemperne ved HPLC?Højtydende væskekromatografi (HPLC) er en laboratorieteknologi, der bruges til at adskille og identificere forbindelser. Det er en type søjlekromatografi, der er afhængig af forskellige polariteter af
Hvad er ulemperne ved HPLC?Højtydende væskekromatografi (HPLC) er en laboratorieteknologi, der bruges til at adskille og identificere forbindelser. Det er en type søjlekromatografi, der er afhængig af forskellige polariteter af -
 Calcium-katalyserede reaktioner af element-H-bindingerKredit:CC0 Public Domain Calcium (Ca) er et af de mest udbredte grundstoffer på jorden, og det er let tilgængeligt og meget billigt. I sammenligning med overgangsmetalelementer, Ca er biokompatibe
Calcium-katalyserede reaktioner af element-H-bindingerKredit:CC0 Public Domain Calcium (Ca) er et af de mest udbredte grundstoffer på jorden, og det er let tilgængeligt og meget billigt. I sammenligning med overgangsmetalelementer, Ca er biokompatibe -
 Forskere bruger neurale netværk til lugtgenkendelseKredit:National Research University Higher School of Economics Forskere fra HSE Laboratory of Space Research, Teknologier, Systemer og processer har anvendt hurtigt lærende kunstige intelligenssys
Forskere bruger neurale netværk til lugtgenkendelseKredit:National Research University Higher School of Economics Forskere fra HSE Laboratory of Space Research, Teknologier, Systemer og processer har anvendt hurtigt lærende kunstige intelligenssys
- Gletsjersmeltning for at omdirigere Alaskas Alsek-flod, fare for verdensberømte raftingrute
- Lekima bliver Supertyphoon, på vej mod det østlige Kina
- Energiniveauer i det periodiske system
- Hubble ser, hvordan en kæmpe planet vokser
- Hvad gør denne video af ting, der smelter så tilfredsstillende?
- Undersøgelse finder tropisk cyklon Winston beskadiget fiskeri samt hjem i Fiji


