Varmebehandling kan gøre kemoterapi mere effektiv
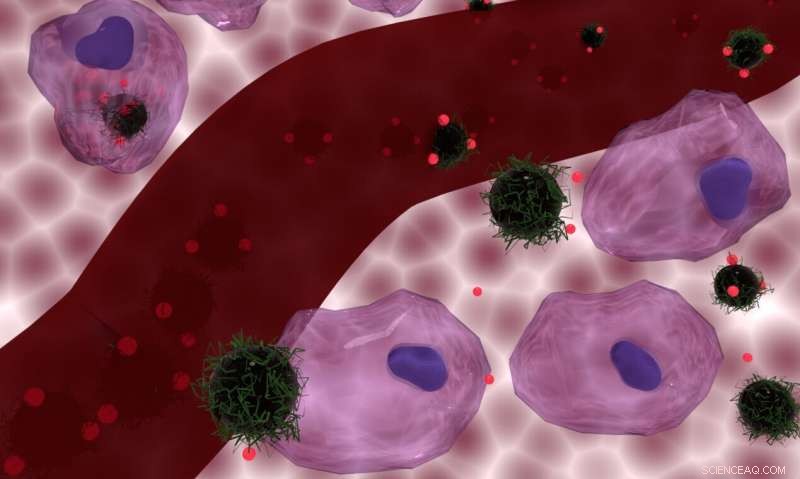
En kunstners opfattelse af, at de doxorubicinfyldte nanokompositbærere internaliseres af celler (øverst) og forbliver udvendige celler (nederst), med en blodåre i midten. Kredit: Journal of Materials Chemistry B / Nguyen T. K. Thanh / Florian Aubrit / Olivier Sandre / Lilin Wang
Opvarmning af kræftceller, mens man målretter dem med kemoterapi, er en yderst effektiv måde at dræbe dem på. ifølge en ny undersøgelse ledet af UCL-forskere.
Studiet, offentliggjort i Journal of Materials Chemistry B , fandt ud af, at det at 'loade' et kemoterapipræparat på små magnetiske partikler, der kan varme kræftcellerne op, samtidig med at stoffet blev leveret til dem, var op til 34 % mere effektivt til at ødelægge kræftcellerne end kemoterapilægemidlet uden tilført varme.
De magnetiske jernoxidnanopartikler, der bærer kemoterapilægemidlet, afgiver varme, når de udsættes for et vekslende magnetfelt. Det betyder at, når nanopartiklerne har samlet sig i tumorområdet, et vekslende magnetfelt kan påføres uden for kroppen, tillader varme og kemoterapi at blive leveret samtidigt.
Effekterne af de to behandlinger var synergistiske - dvs. hver behandling øgede effektiviteten af den anden, hvilket betyder, at de var mere potente, når de kombineres, end når de var adskilte. Undersøgelsen blev udført på celler i et laboratorium, og der er behov for yderligere forskning forud for kliniske forsøg med patienter.
Seniorforfatter professor Nguyen T.K. Thanh (Biophysics Group, UCL Physics &Astronomy) sagde:"Vores undersøgelse viser det enorme potentiale ved at kombinere kemoterapi med varmebehandling leveret via magnetiske nanopartikler.
"Mens denne kombination af terapi allerede er godkendt til behandling af hurtigtvoksende glioblastomer, vores resultater tyder på, at det har potentiale til at blive brugt mere bredt som en bred kræftbehandling.
"Denne terapi har også potentiale til at reducere bivirkningerne af kemoterapi, ved at sikre, at den i højere grad er målrettet mod kræftceller frem for sundt væv. Dette skal undersøges i yderligere prækliniske tests."
I undersøgelsen, forskere kombinerede de magnetiske nanopartikler med et almindeligt anvendt kemoterapimiddel, doxorubicin, og sammenlignede virkningerne af denne komposit i forskellige scenarier på humane brystkræftceller, glioblastom (hjernekræft) celler, og museprostatacancerceller.
I det mest succesrige scenarie, de fandt ud af, at varme og doxorubicin tilsammen dræbte 98 % af hjernekræftcellerne efter 48 timer, når doxorubicin uden varme dræbte 73 %. I mellemtiden for brystkræftceller, 89% blev dræbt af varme og doxorubicin sammen, mens 77% blev dræbt efter 48 timer af doxorubicin alene.
Kræftceller er mere modtagelige for varme end raske celler - de gennemgår en langsom død (apoptose), når temperaturen når 42 grader Celsius, hvorimod raske celler er i stand til at modstå temperaturer op til 45 grader Celsius.
Forskerne fandt ud af, at opvarmning af kræftceller med kun et par grader, til 40 grader Celsius, forbedret effektiviteten af kemoterapien, hvilket betyder, at behandlingen kunne være effektiv med lavere doser af nanopartikler.
De fandt ud af, at kombinationen af terapier var mest effektiv, når nanopartiklerne blev absorberet, eller internaliseret, af kræftcellerne, men de fandt ud af, at kemoterapien også blev forbedret, når nanopartiklerne afgiver varme, mens de forbliver uden for kræftcellerne (hvilket ville være en lettere form for behandling at levere). Imidlertid, virkningerne ved lavere temperaturer opstod kun, når jernoxidnanopartiklerne blev internaliseret eller tæt aflejret på overfladen af kræftcellerne.
Nanopartiklerne har også en polymerbelægning, der forhindrer kemoterapien i at udvaskes i sundt væv. Belægningen er varme- og pH-følsom, og er designet til at frigive lægemidlet, når temperaturen stiger, og nanopartiklerne internaliseres i små lommer i celler kaldet "lysosomer", som har en lavere pH end resten af cellemediet. Denne intracellulære levering af lægemidlet var særligt effektiv for museprostatacancerceller, som viste overlegen og synergetisk celledødseffekt, især når temperaturen nåede 42°C.
Medforfatter Dr. Olivier Sandre, ved universitetet i Bordeaux, sagde:"Da varme kan genereres gennem det vekslende magnetfelt, frigivelsen af lægemidlet kan være stærkt lokaliseret til kræftceller, potentielt reducere bivirkninger."
 Varme artikler
Varme artikler
-
 Mikrostænger lavet af lanthanoide organiske rammer fungerer som optiske bølgeledere i mikroskalaKredit:Wiley Optisk datatransmission gør det muligt at transmittere information som lys ved hjælp af optiske bølgeledere i fiberoptiske netværk. Kinesiske forskere har nu udviklet optiske bølgeled
Mikrostænger lavet af lanthanoide organiske rammer fungerer som optiske bølgeledere i mikroskalaKredit:Wiley Optisk datatransmission gør det muligt at transmittere information som lys ved hjælp af optiske bølgeledere i fiberoptiske netværk. Kinesiske forskere har nu udviklet optiske bølgeled -
 Voksende krystaller til at generere tilfældige talKredit: Stof (2020). DOI:10.1016/j.matt.2020.01.024 Et team ved University of Glasgow har udviklet en ny måde at generere tilfældige tal ved at bruge tilfældigheden i krystalvækst. I deres papir
Voksende krystaller til at generere tilfældige talKredit: Stof (2020). DOI:10.1016/j.matt.2020.01.024 Et team ved University of Glasgow har udviklet en ny måde at generere tilfældige tal ved at bruge tilfældigheden i krystalvækst. I deres papir -
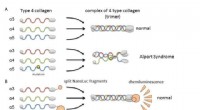 Et meget følsomt og multianalytisk system til arvelig nyresygdom(A) Kollagen IV alfa-3, alfa-4, og alfa-5 danner normalt komplekser (trimere) og bliver bestanddele af basalmembranen i nyren. Ved Alport syndrom, genetisk mutation i en af kæderne forstyrrer trimer
Et meget følsomt og multianalytisk system til arvelig nyresygdom(A) Kollagen IV alfa-3, alfa-4, og alfa-5 danner normalt komplekser (trimere) og bliver bestanddele af basalmembranen i nyren. Ved Alport syndrom, genetisk mutation i en af kæderne forstyrrer trimer -
 Benchmarks for bedre at fange solenYuliar Firdaus og kolleger har udviklet en beregningsmetode til at forudsige effektivitetsgrænser og foreslå designregler for ikke-fulleren organiske solceller. Kredit:King Abdullah University of Scie
Benchmarks for bedre at fange solenYuliar Firdaus og kolleger har udviklet en beregningsmetode til at forudsige effektivitetsgrænser og foreslå designregler for ikke-fulleren organiske solceller. Kredit:King Abdullah University of Scie
- Nanopartikel taxa-materialer kan identificere, opsamle og transportere affald på overflader
- Vellykket test for NASAs gigantiske måneraket
- Det overraskende miljø i en gådefuld neutronstjerne
- Kemikere udfører kirurgi på nanopartikler
- Forskere skaber brandhæmmende sensorer til sikkerhedsudstyr i barske miljøer
- Hvordan man fortæller, om en krystal er diamant eller kvarts?


