Ny bioink bringer 3D-print af menneskelige organer tættere på virkeligheden
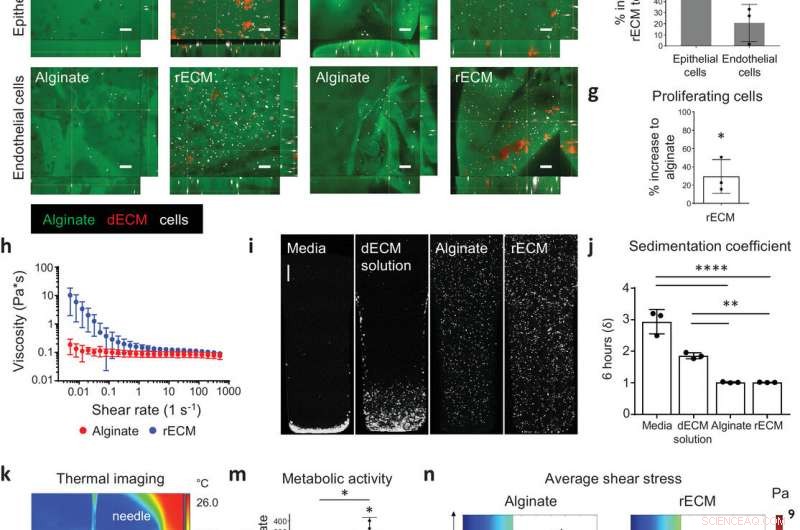
Karakterisering af rECM hybrid hydrogeler. a) Billede af alginat og mus rECM hydrogeler. Målestænger:1 mm. b) Alginat – fluorescein- og ECM – rhodamin -modificeret rECM -hydrogel, der viser fordelingen af alginat- og ECM -komponenterne i hydrogel (se også Video S1 i understøttende oplysninger). Målestang:200 µm. c) SEM -billede af hydrogeler. Målestænger:50 µm. d) Stamkrydsningsgrad (%) mellem lagrings- og tabsmodulet i alginathydrogeler (2%) og rECM -hydrogeler (2%alginat, 5 mg ml − 1 ECM) (n =3 pr. Gruppe). e) Immunofluorescensbilleder af murine lungeepitel -MLE12 og endotel bEnd3 (celler i hvidt) i alginat -fluorescein (grøn) og ECM -opløsning -rhodamin (rød) modificerede rECM -hydrogeler på dag 0 (seedningsdag) og dag 7. Skalaer:100 µm f) Procent stigning i metabolisk aktivitet af epitelceller (MLE12) og endotelceller (bEnd.3) i rECM -hydrogeler sammenlignet med alginathydrogeler på dag 7 (n =3 pr. Gruppe). g) Procentvis stigning af EdU+ prolifererende murine epitelceller (MLE12) i rECM -hydrogeler sammenlignet med alginathydrogeler på dag 5 (n =3 pr. gruppe). h) Oscillerende reometri (n =3 pr. gruppe). i) Konfokale billeder af cellesedimentering og j) beregnet sedimentationskoefficient (δ) for A549 -celler i DMEM -F12 -cellekulturmedier, alginat, mus -afledt dECM- og rECM -opløsning i 6 timer (n =3 pr. gruppe). Målestang:500 µm. k) Termografi af FRISK udskrivning (se Video S2 i understøttende oplysninger). l) 3D bioprintet rECM hulrør og forgreningsstruktur (se videoer S3 og S4 i understøttende oplysninger). Målestænger:2 mm. m) Metabolisk aktivitet (WST -1 -assay) på dag 7 af seedede (in vitro) og 3D -printede A549 -celler i hydrogeler (n =3 pr. gruppe). n) Gennemsnitlige forskydningsspændingsprofiler af bioinks. Kredit: Avancerede materialer (2020). DOI:10.1002/adma.202005476
Forskere ved Lunds Universitet har designet en ny bioink, der gør det muligt for første gang at 3D-bioprintes små luftveje i menneskelig størrelse. De 3D-printede konstruktioner er biokompatible og understøtter vækst af nye blodkar i det transplanterede materiale. Dette er et vigtigt første skridt i retning af 3D-printende organer. Den nye undersøgelse er blevet offentliggjort i Avancerede materialer .
Kroniske lungesygdomme er den tredje største dødsårsag på verdensplan med en EU -pris på mere end 380 milliarder euro årligt. For mange kroniske sygdomme er der ingen kur, og den eneste mulighed i slutstadiet for patienter er lungetransplantation. Imidlertid, der er ikke nok donorlunger til at imødekomme den kliniske efterspørgsel.
Derfor, forskere ser på måder at øge mængden af lunger til rådighed for transplantation. En tilgang er at fremstille lunger i laboratoriet ved at kombinere celler med et bioteknologisk stillads.
"Vi startede i det små med at fremstille små rør, fordi dette er en funktion, der findes i både luftveje og i lungens vaskulatur. Ved at bruge vores nye bioink med stamceller isoleret fra patientens luftveje, vi var i stand til at bioprint små luftveje, som havde flere lag af celler og forblev åbne over tid, "forklarer Darcy Wagner, lektor og seniorforfatter af undersøgelsen.
Forskerne designede først et nyt bioink (et printbart materiale med celler) til 3D-bioprintning af menneskeligt væv. Bioinket blev fremstillet ved at kombinere to materialer:et materiale afledt af tang, alginat, og ekstracellulær matrix afledt af lungevæv.
Denne nye bioink understøtter det bioprintede materiale i flere faser af dets udvikling mod væv. De brugte derefter bioink til 3D-bioprint af små menneskelige luftveje, der indeholder to typer celler, der findes i menneskelige luftveje. Imidlertid, denne bioink kan tilpasses til enhver vævs- eller organtype.
"Disse næste generations biolinks understøtter også modning af luftvejsstamcellerne til flere celletyper, der findes i voksne menneskelige luftveje, hvilket betyder, at færre celletyper skal udskrives, forenkling af dysenumre, der er nødvendige for at udskrive væv lavet af flere celletyper, "siger Darcy Wagner.
Wagner bemærker, at opløsningen skal forbedres til 3D-bioprint mere distalt lungevæv og luftsækkene, kendt som alveoler, der er afgørende for gasudveksling.
"Vi håber, at yderligere teknologiske forbedringer af tilgængelige 3D -printere og yderligere bioink -fremskridt vil give mulighed for bioprintning ved en højere opløsning for at konstruere større væv, som kan bruges til transplantation i fremtiden. Vi har stadig en lang vej at gå, " hun siger.
Teamet brugte en musemodel, der meget lignede den immunsuppression, der blev brugt hos patienter, der gennemgik organtransplantation. Ved transplantation, de fandt ud af, at 3D-printede konstruktioner fremstillet af den nye bioink tolereredes godt og understøttede nye blodkar.
"Udviklingen af denne nye bioink er et vigtigt skridt fremad, men det er vigtigt at validere de små luftvejers funktionalitet yderligere over tid og undersøge muligheden for denne tilgang i store dyremodeller, "slutter Martina De Santis, undersøgelsens første forfatter.
 Varme artikler
Varme artikler
-
 Stand-up poser fra vedvarende råvarer og nanocelluloseKredit:Technical Research Center of Finland (VTT) VTT Technical Research Center of Finland Ltd har udviklet lette 100% biobaserede stand-up poser med høj teknisk ydeevne. Høj ydeevne i både ilt, f
Stand-up poser fra vedvarende råvarer og nanocelluloseKredit:Technical Research Center of Finland (VTT) VTT Technical Research Center of Finland Ltd har udviklet lette 100% biobaserede stand-up poser med høj teknisk ydeevne. Høj ydeevne i både ilt, f -
 Molekyleundersøgelser afslører potentiel behandling for patienter med slagtilfældeEn tegneserierepræsentation afsløret af undersøgelsen viser den lukkede tilstand af PDZ-domænerne. Kredit: Naturkommunikation , doi:10.1038/s41467-018-06133-0 I en forlængelse af forskning offent
Molekyleundersøgelser afslører potentiel behandling for patienter med slagtilfældeEn tegneserierepræsentation afsløret af undersøgelsen viser den lukkede tilstand af PDZ-domænerne. Kredit: Naturkommunikation , doi:10.1038/s41467-018-06133-0 I en forlængelse af forskning offent -
 Teknologien bruger plantebiomasseaffald til selvdrevne biomedicinske enhederWenzhuo Wu, Ravi og Eleanor Talwar Rising Star, assisterende professor i industriteknik ved Purdues College of Engineering, er en innovator med fokus på at finde løsninger på tværs af flere discipline
Teknologien bruger plantebiomasseaffald til selvdrevne biomedicinske enhederWenzhuo Wu, Ravi og Eleanor Talwar Rising Star, assisterende professor i industriteknik ved Purdues College of Engineering, er en innovator med fokus på at finde løsninger på tværs af flere discipline -
 Bevæg dig over tunge beskyttelsesbriller, her kommer de ultrahøje brydningsindekslinserKredit:Pohang University of Science &Technology (POSTECH) Et POSTECH-forskerhold har udviklet et gennemsigtigt amorft silicium, der transmitterer synligt lys-hvilket gør det muligt for os at skeln
Bevæg dig over tunge beskyttelsesbriller, her kommer de ultrahøje brydningsindekslinserKredit:Pohang University of Science &Technology (POSTECH) Et POSTECH-forskerhold har udviklet et gennemsigtigt amorft silicium, der transmitterer synligt lys-hvilket gør det muligt for os at skeln
- Hvad gør denne video af ting, der smelter så tilfredsstillende?
- Ægfaldskærmdesigninstruktioner
- Den varmeste maj nogensinde, Sibirien 10C varmere
- GE tabte milliarder ved at fejlvurdere vedvarende energi:rapport
- Matematik kaster lys over, hvordan levende celler tænker
- Nanoskala fotodetektor viser løfte om at forbedre kapaciteten af fotoniske kredsløb


