Forskere får ny indsigt i et dynamisk protein målrettet mod kræftbehandling

Grafisk abstrakt. Kredit:Élise Rouleau-Turcotte et al., Molecular Cell (2022). DOI:10.1016/j.molcel.2022.06.011
Ny strukturel information om et enzymmål i kræftmedicin kan hjælpe med udviklingen af næste generations inhibitorer. Enzymet, kaldet PARP1, registrerer DNA-skade og sender et cellulært signal til at udføre reparation. PARP1-aktivitet er vigtig for mange kræfttyper, hvilket gør det til et attraktivt mål for behandlinger.
Kliniske undersøgelser har vist, at PARP1-hæmmere kan bruges som antitumorbehandlinger, der virker ved at forstyrre DNA-replikation og reparation for at dræbe kræftceller. For nylig er forskere begyndt at undersøge, om PARP1 også kan bruges som et mål i behandlinger af andre sygdomme, herunder Alzheimers og Parkinsons sygdom, hvor reduktionen i PARP1-hyperaktivitet kan hjælpe celler med at overleve.
For første gang har forskere fra Université de Montréal og Institute of Cancer Research i Storbritannien fanget et "snapshot" af PARP1 i den aktive tilstand, som det adopterer efter at have opdaget DNA-skader. Holdets nye forskning, offentliggjort i tidsskriftet Molecular Cell , fremmer vores forståelse af, hvordan disse enzymer opfører sig og baner vejen for den næste generation af PARP1-hæmmere.
Røntgendiffraktionsdataene, der gav disse indsigter, blev opnået ved hjælp af CMCF-strålelinjen ved den canadiske lyskilde (CLS) ved University of Saskatchewan og den avancerede lyskilde i USA
Den region af PARP1, som hæmmere angreb, er ret mobil, hvilket gør det vanskeligt fuldt ud at forstå dette bevægelige mål, sagde Dr. John Pascal, professor ved Institut for Biokemi og Molekylær Medicin ved Université de Montréal og medlem af dette forskerhold.
Visse hæmmere engagerer de dynamiske områder af PARP1 og kan fungere som en skruenøgle, der sidder fast i et hjul eller som en dørstop under en dør, hvilket effektivt hjælper med at låse PARP1 på DNA-skader, forklarede Pascal. "Denne hæmningsmåde kunne forbedre mekanismen til at dræbe kræftceller." I modsætning hertil kunne inhibitorer, der undgår de dynamiske regioner og mangler "doorstop"-effekten, være bedre egnede til neurodegenerative sygdomme, hvor cellebevarelse er målet frem for celledrab. + Udforsk yderligere
Forskere identificerer nyt relevant mål for PARP-hæmmeren talazoparib
 Varme artikler
Varme artikler
-
 Teoretisk forudsigelse af omvendt intersystemkrydsning for organiske halvledereKredit:CC0 Public Domain Et fælles forskerhold ved RIKEN og Hokkaido University udviklede en metode til at forudsige hastighedskonstanter for reverse intersystem crossing (RISC) forbundet med lyse
Teoretisk forudsigelse af omvendt intersystemkrydsning for organiske halvledereKredit:CC0 Public Domain Et fælles forskerhold ved RIKEN og Hokkaido University udviklede en metode til at forudsige hastighedskonstanter for reverse intersystem crossing (RISC) forbundet med lyse -
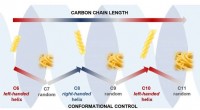 Kulstofkæder antager fusilli- eller spaghetti-former, hvis de har ulige eller lige talBilledet viser, hvordan konformationen (formen) af vores carbonkæder veksler mellem ordnede og kaotiske strukturer, da carbonkæden veksler mellem at have lige og ulige antal atomer. Kredit:University
Kulstofkæder antager fusilli- eller spaghetti-former, hvis de har ulige eller lige talBilledet viser, hvordan konformationen (formen) af vores carbonkæder veksler mellem ordnede og kaotiske strukturer, da carbonkæden veksler mellem at have lige og ulige antal atomer. Kredit:University -
 Undersøgelse afslører en kontinuerlig vej til livets byggestenGenerering af målmolekyler, der er relevante for livets oprindelse i et komplekst kemisk netværk drevet af stråling. Kredit:Ruiqin Yi, ELSI Forskere har længe søgt at forstå oprindelsen af liv p
Undersøgelse afslører en kontinuerlig vej til livets byggestenGenerering af målmolekyler, der er relevante for livets oprindelse i et komplekst kemisk netværk drevet af stråling. Kredit:Ruiqin Yi, ELSI Forskere har længe søgt at forstå oprindelsen af liv p -
 Sådan laver du et skoleprojekt Battlefield DisplayLav et slagmarkskærm til skole, der viser landets geografi samt militærbevægelserne fra soldaterne. Dette projekt kan udfyldes med elementer fundet i de fleste boliger. Hvad der ikke er tilgængeligt h
Sådan laver du et skoleprojekt Battlefield DisplayLav et slagmarkskærm til skole, der viser landets geografi samt militærbevægelserne fra soldaterne. Dette projekt kan udfyldes med elementer fundet i de fleste boliger. Hvad der ikke er tilgængeligt h
- Næste skridt på vejen mod en effektiv biobrændselscelle
- Billede:Taal vulkan dækket af aske
- Asteroide Ryugu sandsynligvis forbindelse i planetarisk formation
- Bahamas blev bosat tidligere end troet, bosættere ændrede dramatisk landskab
- Sentinel-1 gennemskuer orkaner
- NASAs stormdæmpede rover markerer 15 års jubilæum på Mars


