Tyske forskere udvikler en ny mutasyntese-tilgang til derivatisering af antibiotika
En ny metode til derivatisering af antibiotika er udviklet af professor Dr. Yvonne Mast, leder af Institut for Bioressourcer for Bioøkonomi og Sundhedsforskning, og hendes arbejdsgruppe ved Leibniz Instituttet DSMZ-German Collection of Microorganisms and Cell Cultures.
Antibiotika er medicinsk vigtige forbindelser, der ofte produceres af mikroorganismer. Sådanne naturlige stoffer har ofte en kemisk kompleks struktur og kan derfor være vanskelige eller endda umulige at syntetisere eller modificere kemisk ved hjælp af semisyntese. Det er dog ofte nødvendigt at tilpasse disse stoffer for at forbedre effektiviteten eller, som i tilfældet med antibiotika, for at give resistensbrydende egenskaber.
Mutasyntese tilbyder et alternativ til kemisk modifikation eller "derivatisering" af stoffer. Denne tilgang genererer mutanter af antibiotika-producerende mikroorganismer, hvor generne for antibiotikumprecursoren(erne) inaktiveres, så mikroorganismen ikke længere kan producere dem.
Ved at "fodre" mutanter med modificerede præprodukter (precursor-derivaterne), inkorporeres disse derefter i antibiotikum-precursor-molekylet, hvilket resulterer i produktionen af nye antibiotika-derivater.
Mutasyntese:En tilgang til at modificere antibiotika
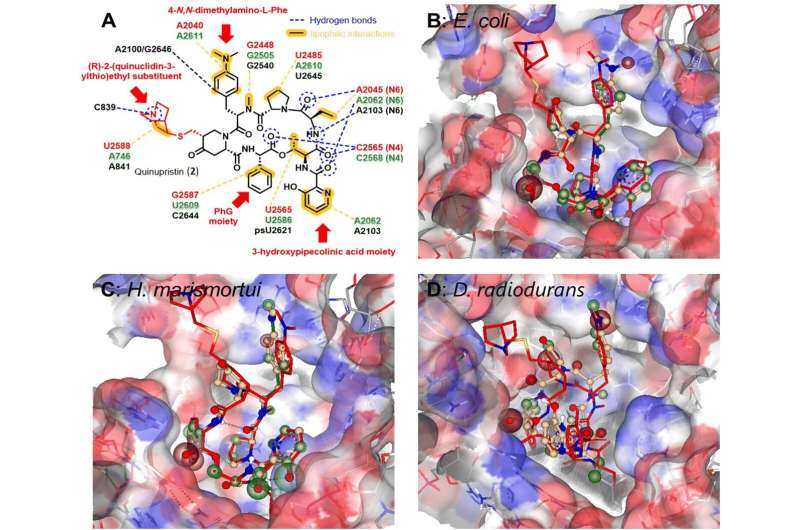
I en undersøgelse for nylig offentliggjort i RSC Chemical Biology , beskriver Prof Masts arbejdsgruppe en ny mutasyntese-tilgang til derivatisering af antibiotikumet pristinamycin I. Pristinamycin er et streptogramin-antibiotikum, der bruges som nødlægemiddel mod resistente patogener.
"Vi modificerede pristinamycin I baseret på aminosyreprecursoren phenylglycin ved mutasyntese," forklarer antibiotikaforsker Yvonne Mast.
"Dette var kun muligt, fordi vi tidligere havde identificeret og funktionelt karakteriseret phenylglycinbiosyntesegenerne, hvilket gjorde det muligt for os at generere to nye halogenerede bioaktive pristinamycin I-derivater i vores nuværende undersøgelse."
"Nyheden i denne undersøgelse ligger i, at vi koblede en biotransformationsproces til mutasyntese, hvor phenylglycinderivatets forstadium leveres af en genetisk modificeret bakteriestamme (E. coli-stamme). Indtil videre er dette den eneste bioteknologiske proces af dens slags, som vi har kaldt mutasynthesis 2.0," siger prof Mast.
Flere oplysninger: Oliver Hennrich et al., Biotransformationskoblet mutasyntese til dannelse af nye pristinamycinderivater ved at manipulere phenylglycinresten, RSC Chemical Biology (2023). DOI:10.1039/D3CB00143A
Leveret af Leibniz-Institut DSMZ-Deutsche Sammlung von Mikroorganismen und Zellkulturen GmbH
 Varme artikler
Varme artikler
-
 Nanoteknologi gør det muligt for ingeniører at svejse tidligere usvejsbare aluminiumslegeringerTo stykker aluminiumslegering 7075 svejset sammen ved hjælp af en nanopartikel-forstærket fyldtråd. Kredit:Oszie Tarula/UCLA En aluminiumslegering udviklet i 1940erne har længe holdt et løfte til
Nanoteknologi gør det muligt for ingeniører at svejse tidligere usvejsbare aluminiumslegeringerTo stykker aluminiumslegering 7075 svejset sammen ved hjælp af en nanopartikel-forstærket fyldtråd. Kredit:Oszie Tarula/UCLA En aluminiumslegering udviklet i 1940erne har længe holdt et løfte til -
 En ny måde at fremstille MXene-film på, der blokerer for elektromagnetisk interferensMed boomet i bærbar elektronik, Internet of Things-enheder og mere, belægninger, der blokerer for elektromagnetisk stråling, er ved at blive en kritisk del af fremstillingsprocessen. Andre ́ D. Taylor
En ny måde at fremstille MXene-film på, der blokerer for elektromagnetisk interferensMed boomet i bærbar elektronik, Internet of Things-enheder og mere, belægninger, der blokerer for elektromagnetisk stråling, er ved at blive en kritisk del af fremstillingsprocessen. Andre ́ D. Taylor -
 Genetisk årsag til ALS og frontotemporal demens blokeret af RNA-bindende forbindelseScripps Research Chemistry Professor Matthew Disney, Ph.d., går over en formel i sit laboratorium. Hans gruppe på Scripps Research i Jupiter, Florida har lavet et potentielt lægemiddel, der stopper AL
Genetisk årsag til ALS og frontotemporal demens blokeret af RNA-bindende forbindelseScripps Research Chemistry Professor Matthew Disney, Ph.d., går over en formel i sit laboratorium. Hans gruppe på Scripps Research i Jupiter, Florida har lavet et potentielt lægemiddel, der stopper AL -
 Nær-infrarød sonde afkoder telomerdynamikEn fluorescerende forbindelse blev knyttet til PIPet, der er målrettet mod den gentagne DNA -sekvens, der findes i telomerer. Denne sonde, kaldet SiR-TTet59B, muliggør observation af telomerer i aktio
Nær-infrarød sonde afkoder telomerdynamikEn fluorescerende forbindelse blev knyttet til PIPet, der er målrettet mod den gentagne DNA -sekvens, der findes i telomerer. Denne sonde, kaldet SiR-TTet59B, muliggør observation af telomerer i aktio
- Astronomer bygger et 3D-kort af støv inden for tusindvis af lysår
- Omdannelse af kuldioxid til methanol
- Nanorør katode slår stort, dyr laser
- Hvad er en subtropisk storm, og hvordan adskiller den sig fra et tropisk eller ekstratropisk system?…
- NASA ser en styrkelse og svækkelse af den tropiske depression Beatriz
- America's Next Top Model:Hvordan bidrager fans til nedgangen for deres yndlings-tv-shows?


