Mineralcoatinger kunne muliggøre opbevaringsstabile mRNA-terapier
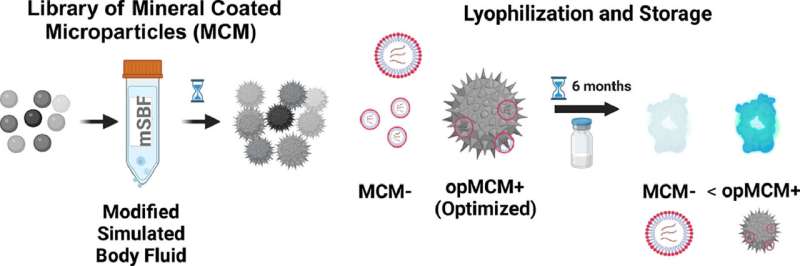
En beskyttende mineralbelægning identificeret af University of Wisconsin-Madison biomedicinske ingeniørforskere kunne tillade, at kraftfulde budbringer-RNA-terapier som COVID-19-vacciner opbevares ved stuetemperatur, hvilket gør dem mere tilgængelige for samfund med lavere ressourcer over hele verden.
I et papir offentliggjort i tidsskriftet Acta Biomaterialia , Professor William Murphy og samarbejdspartnere i hans laboratorium detaljerede, hvordan brug af en optimeret mineralcoatingsammensætning kan opretholde mRNA-aktivitet i op til seks måneder ved stuetemperatur. Med den form for konservering kunne mRNA-terapi – vacciner mod infektionssygdomme, men også nye behandlinger for cancer og vævsregenerering – opbevares på hylden på lokale klinikker.
Den hurtige udvikling af mRNA-baserede COVID-19-vacciner var en game-changer i pandemien. Vaccinerne anvender mRNA til at dirigere celler til at producere et protein fra overfladen af virussen, hvilket udløser et immunrespons, der forbereder vores kroppe til den ægte vare.
Flere skøn viser, at vaccinerne, et resultat af årtiers trinvis mRNA-forskning – hvoraf nogle resulterede i en Nobelpris i 2023 – reddede millioner af liv.
Der er kun ét problem:COVID-19-vaccinerne, såvel som andre mRNA-baserede behandlinger mod kræft, kræver kølekædelagring for at bevare deres styrke.

"Det lyder som et trivielt problem, men det er faktisk et ganske enormt problem," siger Murphy, professor i biomedicinsk teknik og ortopædi og rehabilitering. "Hvis du forsøger at få disse til Afrika syd for Sahara, vil du få betydelige udfordringer."
Studieleder Joshua Choe, en MD-Ph.D. studerende i Murphys laboratorium, screenede 40 mineralsammensætninger med det formål at finde en, der, når den kombineres med mRNA-komplekser, optimerer deres stabilitet i enklere formuleringer end dem, der bruges til nuværende vacciner.
Til sidst identificerede han en sammensætning med en passende mængde citrat og fluorid, der bibeholdt styrken af frysetørret mRNA. Han anvender nu tilgangen til lignende formuleringer som dem, der bruges i COVID-vacciner med lovende tidlige resultater. Gruppen har indsendt et foreløbigt patent baseret på arbejdet gennem Wisconsin Alumni Research Foundation.
"Hele vejen til seks måneder bevarer du den aktivitet, mens du uden at bruge vores mineral til at opbevare disse mRNA-terapier mister en del af aktiviteten efter to uger, og så falder den til næsten ingenting," siger Choe, der håber på at arbejde som ortopædkirurg og forsker efter endt uddannelse.
Tilgangen henter inspiration fra gamle fossilers dokumenterede evne til at bevare DNA og proteiner. Forskere har med succes udvundet DNA for at analysere genomet af "Denny", en anslået 90.000 år gammel forfader til mennesker, hvis rester blev fundet i en russisk hule i 2012. I et andet fund i Tanzania fandt forskere intakte proteiner i strudseæggeskaller, der dateres til 3,8 millioner år siden.
Murphys laboratorium har brugt mineraler til at stabilisere biologiske molekyler til forskellige biomedicinske anvendelser i omkring 15 år, og Choe så en mulighed for at anvende taktikken til mRNA-terapi, mens han arbejdede i laboratoriet i de isolerede dage af vinteren 2020.
Ud over yderligere at demonstrere deres tilgangs effektivitet med mRNA-vacciner, fortsætter Murphy og hans gruppe brugen af det til vævsregenerering, især til behandling af rygmarvsskader, sårheling og genvækst af brusk, muskler og knogler.
"Vi ønsker at være i stand til at opnå det på en måde, der kommer fra hylden, så du bogstaveligt talt kan tage en behandling fra hylden, påføre den på en patient og stimulere vævsregenerering," siger Murphy.
William Murphy er Harvey D. Spangler-professor og H.I. Romnes fakultetsstipendiat. Han er også den stiftende direktør for Forward BIO Institute ved UW-Madison. Andre forfattere på papiret omfatter Murphy lab medlemmer Hannah Brinkman, en DVM/Ph.D. studerende og Jae Sung Lee, en stabsforsker.
Flere oplysninger: Joshua A. Choe et al., Optimized Biomimetic Minerals Maintain Activity of mRNA Complexes after Long Term Storage, Acta Biomaterialia (2023). DOI:10.1016/j.actbio.2023.11.044
Journaloplysninger: Acta Biomaterialia
Leveret af University of Wisconsin-Madison
 Varme artikler
Varme artikler
-
 Forsker arbejder på at forstå, hvordan gonoré udvikler resistens over for antibiotikaDette billede genereret ved røntgenkrystallografi viser et cephalosporin-antibiotikum, i pink, binding til et protein fra bakterien, der forårsager gonoré. Kuglerne repræsenterer vandmolekyler. Kredit
Forsker arbejder på at forstå, hvordan gonoré udvikler resistens over for antibiotikaDette billede genereret ved røntgenkrystallografi viser et cephalosporin-antibiotikum, i pink, binding til et protein fra bakterien, der forårsager gonoré. Kuglerne repræsenterer vandmolekyler. Kredit -
 Vurdering af begyndelsen af calciumphosphatkernen ved hyperpolariseret real-time NMRFor at skabe effektive funktionelle materialer, naturen tilbyder de bedste opskrifter ved at levere evolutionært vellykkede koncepter, siger Dennis Kurzbach fra Institut for Biologisk Kemi. Kredit:© S
Vurdering af begyndelsen af calciumphosphatkernen ved hyperpolariseret real-time NMRFor at skabe effektive funktionelle materialer, naturen tilbyder de bedste opskrifter ved at levere evolutionært vellykkede koncepter, siger Dennis Kurzbach fra Institut for Biologisk Kemi. Kredit:© S -
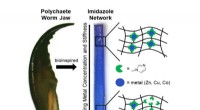 Forskere efterligner en ormedødelig kæbe for at designe og danne elastiske materialerForskere skabte en bioinspireret gradient i mekaniske egenskaber. Området opnås ved at programmere tætheden af en speciel interaktion mellem metalioner og elektrondonerende ligander. Det venstre bil
Forskere efterligner en ormedødelig kæbe for at designe og danne elastiske materialerForskere skabte en bioinspireret gradient i mekaniske egenskaber. Området opnås ved at programmere tætheden af en speciel interaktion mellem metalioner og elektrondonerende ligander. Det venstre bil -
 At forstå, hvordan en katalysator omdanner metan til ethen, kan forhindre flaring af naturgasDeponi brænder flare af. Kredit:Eddie Hagler/Public Domain Det ville være en tredobbelt sejr - for klimaet, råmaterialeressourcer, og den kemiske industri. Med deres arbejde, videnskabsfolk ved Fr
At forstå, hvordan en katalysator omdanner metan til ethen, kan forhindre flaring af naturgasDeponi brænder flare af. Kredit:Eddie Hagler/Public Domain Det ville være en tredobbelt sejr - for klimaet, råmaterialeressourcer, og den kemiske industri. Med deres arbejde, videnskabsfolk ved Fr
- Hvem betaler for din Uber?
- Dyr i fangenskab viser tegn på kedsomhed, viser undersøgelser
- Oplysninger om langsigtet permafrost Arktisk tø
- NASA fanger Post Tropical Cyclone Cosme fading
- Brug af en quantum blockchain til at beskytte fremtidens blockchains
- Forskeren ønsker at lægge magten til at modellere luftforurening i dine hænder


