Atom-for-atom-opløsning registreret for første gang
Et team af kemikere og fysikere ved Aarhus Universitet, i Danmark, i samarbejde med en kollega fra Universitat de Barcelona i Spanien, har for første gang registreret atom-for-atom-opløsning. I deres undersøgelse, offentliggjort i tidsskriftet Nature , designet gruppen en proces til at manipulere natrium- og xenonatomer med en dråbe helium ved meget kolde temperaturer for at fange, hvad de beskriver som øjebliksbilleder af solvationsprocessen over tid. Tilsammen producerer disse en film, der skildrer handlingen. En forskningsbriefing om arbejdet er blevet publiceret i samme tidsskriftsnummer.
Solvation er opløsning af et opløst stof i et opløsningsmiddel - når salt for eksempel opløses i vand. Handlingen stopper ikke bare fordi det opløste stof er opløst; i stedet fortsætter opløsningsmidlerne med at interagere med det materiale, der er blevet opløst.
Tidligere forskning har vist, at sådanne interaktioner kan være ret komplicerede, og derfor vil kemikere gerne vide mere om, hvad der sker. En måde at finde ud af det på ville være at filme handlingen og spille den som en film. Dette enkle koncept har dog vist sig at være usædvanligt svært - så svært, at det ikke blev gennemført før for nylig af holdet i Danmark.
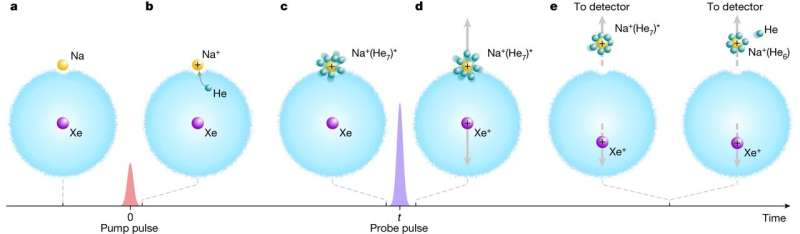
For at opnå deres bedrift begyndte forskerne med at fange et enkelt xenonatom inde i en dråbe flydende helium, der var blevet afkølet til -255°C og derefter tilføje et enkelt natriumatom til den ydre kant af dråben. De affyrede en kort puls fra en laser mod natriumatomet for at omdanne det til en positivt ladet ion, hvilket satte solvatisering i gang – heliumatomerne begyndte at klæbe til natriumionen.
Holdet affyrede derefter endnu en laserimpuls, denne gang mod xenonatomet, og ændrede det til en positivt ladet ion. De to ioner frastødte hinanden i en sådan grad, at natriumionen med dens vedhæftede heliumatomer blev skubbet ud af dråben og ind på en detektor, som gjorde det muligt at fange et øjebliksbillede af, hvad der foregik.
Forskerne gentog derefter processen, hver gang de ventede længere med at udløse den anden puls. De var i stand til at skabe, hvad de beskriver som progressive øjebliksbilleder af handlingen. Så, når de havde fået flere sekventielle snapshots, syede de dem sammen for at skabe en film, der skildrede løsningsprocessen i aktion.
Flere oplysninger: Simon H. Albrechtsen et al, Observation af de primære trin af ionopløsning i heliumdråber, Nature (2023). DOI:10.1038/s41586-023-06593-5
Heliumdråber hjælper med at visualisere starten på ionopløsning, Nature (2023). DOI:10.1038/d41586-023-02950-6
Journaloplysninger: Natur
© 2023 Science X Network
Sidste artikelAt skubbe grænserne for gassensorteknologi
Næste artikelKemikere billede grundlæggende blokke af syntetiske polymerer
 Varme artikler
Varme artikler
-
 Undervisning i gamle overgangsmetaller nye tricks:Kemikere aktiverer palladiumkatalyse ved lysKemisk illustration af den nye metode til fremstilling af π-allylpalladiumkomplekser ved radikal kemi Kredit:Frank Glorius Ved fremstilling af forbindelser, kemikere har det grundlæggende mål at f
Undervisning i gamle overgangsmetaller nye tricks:Kemikere aktiverer palladiumkatalyse ved lysKemisk illustration af den nye metode til fremstilling af π-allylpalladiumkomplekser ved radikal kemi Kredit:Frank Glorius Ved fremstilling af forbindelser, kemikere har det grundlæggende mål at f -
 En grænsedans for amyloid-β, der træder ind i demens(a) Et Aβ-peptid, der danner en β-hårnålestruktur ved den hydrofile/hydrofobe grænseflade. (b) Udsigt fra bunden af panelet (a). Kredit:ExCELLS/IMS Alzheimers sygdom er forårsaget af aggregater
En grænsedans for amyloid-β, der træder ind i demens(a) Et Aβ-peptid, der danner en β-hårnålestruktur ved den hydrofile/hydrofobe grænseflade. (b) Udsigt fra bunden af panelet (a). Kredit:ExCELLS/IMS Alzheimers sygdom er forårsaget af aggregater -
 Lipid-baserede grænsesmurte hydrogeler viste sig at være glattere end dem, der er baseret på vandMikroreservoirerne af lipidvesikler i hovedparten af hydrogelen, som det ses ved scanningselektronmikroskopi, når gelen brydes ved lave temperaturer for at blotlægge en indre overflade. Kredit:Lin e
Lipid-baserede grænsesmurte hydrogeler viste sig at være glattere end dem, der er baseret på vandMikroreservoirerne af lipidvesikler i hovedparten af hydrogelen, som det ses ved scanningselektronmikroskopi, når gelen brydes ved lave temperaturer for at blotlægge en indre overflade. Kredit:Lin e -
 En løsning på et behåret problem inden for retsmedicinMenneskehår består af proteiner kaldet keratiner, der er viklet sammen til en holdbar struktur. Kredit:N. Hanacek/NIST I et forsøg på at gøre hårsammenligning til en mere nyttig teknik til at efte
En løsning på et behåret problem inden for retsmedicinMenneskehår består af proteiner kaldet keratiner, der er viklet sammen til en holdbar struktur. Kredit:N. Hanacek/NIST I et forsøg på at gøre hårsammenligning til en mere nyttig teknik til at efte
- Udvikling af bedre fremstillingsteknikker til pH-responsive mikrokapsler
- Klare lys af renhed:Forskere opdager, hvorfor rene kvanteprikker og nanorods skinner klarere
- De fleste konstruerede nanopartikler trænger ind i tumorer gennem celler, ikke mellem dem
- iPhone 11:Hvad kan du forvente, og hvorfor ventetid kan være din bedste mulighed
- Kun otte EU-lande skal udfase kul inden 2030
- Tilstoppede porer for øget effektivitet:Valleprotein stabiliserer nanotransporter, kontrollerer pH-…


