Hvordan det periodiske system fungerer
Det periodiske system af grundstoffer er et tabelarrangement af de kemiske grundstoffer, organiseret på basis af deres atomnummer, elektronkonfiguration og tilbagevendende kemiske egenskaber. Tabellens struktur viser periodiske tendenser i grundstoffernes egenskaber som funktion af deres atomnummer.
Atomnummer
Et grundstofs atomnummer er antallet af protoner i dets kerne. Det er en unik identifikator for hvert grundstof, og den bestemmer grundstoffets plads i det periodiske system.
Elektronkonfiguration
Elektronkonfigurationen af et element beskriver arrangementet af elektroner i dets orbitaler. Elektronkonfigurationen bestemmer grundstoffets kemiske egenskaber.
Periodiske tendenser
Det periodiske system viser flere periodiske tendenser i grundstoffernes egenskaber. Disse tendenser omfatter:
* Atomradius: Atomradius er afstanden fra kernen til den yderste elektronskal. Det falder generelt over en periode og stiger ned ad en gruppe.
* Ioniseringsenergi: Ioniseringsenergien er den energi, der kræves for at fjerne den yderste elektron fra et atom. Det stiger generelt over en periode og falder ned ad en gruppe.
* Elektronegativitet: Elektronegativitet er et atoms evne til at tiltrække elektroner. Det stiger generelt over en periode og falder ned ad en gruppe.
Det periodiske system og kemi
Det periodiske system er et grundlæggende værktøj til at forstå grundstoffernes kemi. Det kan bruges til at forudsige de kemiske egenskaber af et grundstof baseret på dets placering i tabellen. Det periodiske system bruges også til at organisere og klassificere kemiske reaktioner.
Betydningen af det periodiske system
Det periodiske system er et af de vigtigste videnskabelige værktøjer, der nogensinde er skabt. Det bruges af kemikere, fysikere, biologer og andre videnskabsmænd til at forstå stoffets egenskaber. Det periodiske system er også et værdifuldt pædagogisk værktøj, da det kan hjælpe eleverne til at lære om de forskellige grundstoffer og deres egenskaber.
Sidste artikelHvordan granater virker
Næste artikelSådan fungerer genbrug
 Varme artikler
Varme artikler
-
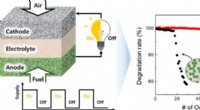 Reduceret nikkelindhold og forbedret stabilitet og ydeevne i keramiske brændselscellerKonceptuelt diagram over oxidations-reduktionscyklus af keramiske brændselsceller og sammenligning af nyt koncept vs. forringelsesrate for konventionelle brændstofplader Kredit:Korea Institute of Scie
Reduceret nikkelindhold og forbedret stabilitet og ydeevne i keramiske brændselscellerKonceptuelt diagram over oxidations-reduktionscyklus af keramiske brændselsceller og sammenligning af nyt koncept vs. forringelsesrate for konventionelle brændstofplader Kredit:Korea Institute of Scie -
 En lettere receptKredit:Pixabay Type I-diabetespatienter injicerer typisk insulin flere gange om dagen, en smertefuld proces, der reducerer livskvaliteten. Injicerbare medicin er også forbundet med manglende overh
En lettere receptKredit:Pixabay Type I-diabetespatienter injicerer typisk insulin flere gange om dagen, en smertefuld proces, der reducerer livskvaliteten. Injicerbare medicin er også forbundet med manglende overh -
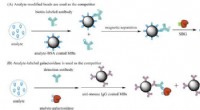 Ny immunoassay-teknik måler ekstremt lave koncentrationer af små molekyler ved hjælp af enkelt-mo…Skematisk illustration af konkurrerende Simoa-assays ved anvendelse af analytmodificerede MBer (A) og analyt-mærket β-galactosidase som konkurrent (B). Kredit:(c) Journal of the American Chemical Soc
Ny immunoassay-teknik måler ekstremt lave koncentrationer af små molekyler ved hjælp af enkelt-mo…Skematisk illustration af konkurrerende Simoa-assays ved anvendelse af analytmodificerede MBer (A) og analyt-mærket β-galactosidase som konkurrent (B). Kredit:(c) Journal of the American Chemical Soc -
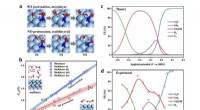 Forskere afslører potentiel afhængighed af nitrogenoxid -elektrisk reduktion til ammoniak(a)-(b) Verifikation af monolagsvandmodel i elektrokatalytiske energibarriereberegninger; (c)-(d) Sammenligning af teoretisk og eksperimentel faradaisk effektivitet. Kredit:LONG Jun Kvælstofoxid (
Forskere afslører potentiel afhængighed af nitrogenoxid -elektrisk reduktion til ammoniak(a)-(b) Verifikation af monolagsvandmodel i elektrokatalytiske energibarriereberegninger; (c)-(d) Sammenligning af teoretisk og eksperimentel faradaisk effektivitet. Kredit:LONG Jun Kvælstofoxid (
- Forskning fremhæver virkningen af recessionen på stress i familier
- Organopbevaring et skridt nærmere med kryokonservering
- Celle-afledte nanobærere til mere effektiv og direkte intracellulær lægemiddelfrigivelse
- Små fossiler afslører spor til jordens klima for en halv milliard år siden
- Forskere finder ud af, at stråling i rummet bliver mere og mere farlig
- Hvordan religioner former miljøbevægelsen i Indonesien


