Hvordan to væsker blandes ved overfladen:et atomsyn
1. Kollision og diffusion:
- Når de to væsker kommer i kontakt, begynder deres molekyler at kollidere med hinanden.
- Kollisionerne fører til overførsel af energi og momentum mellem molekylerne, hvilket får dem til at diffundere ind i hinandens rum.
- Diffusionshastigheden afhænger af væskernes temperatur, viskositet og molekylstørrelse.
2. Intermolekylære kræfter:
- Blandingsadfærden af væsker er også påvirket af intermolekylære kræfter, der virker mellem deres molekyler.
- Væsker med lignende intermolekylære kræfter (f.eks. både polære eller begge ikke-polære) har en tendens til at blandes lettere end væsker med forskellige intermolekylære kræfter.
- For eksempel blandes vand og ethanol, begge polære væsker, let på grund af stærk hydrogenbinding, mens olie og vand, henholdsvis en ikke-polær og polær væske, udviser begrænset blanding på grund af svage intermolekylære interaktioner.
3. Overfladespænding:
- Overfladespænding opstår fra sammenhængskraften mellem molekyler ved væske-luft-grænsefladen.
- Væsker med lavere overfladespænding har en tendens til at spredes lettere og blandes lettere med andre væsker.
- Overfladeaktive stoffer (overfladeaktive midler) kan reducere overfladespændingen og lette blandingen ved at fremme spredningen af en væske i en anden.
4. Molekylær struktur:
- Væskernes molekylære struktur påvirker også deres blandingsadfærd.
- Væsker med mindre molekyler har en tendens til at blande sig lettere end dem med større molekyler.
- Ethanol blander sig for eksempel lettere med vand sammenlignet med olier, som har større og mere komplekse molekylære strukturer.
5. Viskositet:
- Viskositet måler en væskes modstand mod strømning.
- Væsker med lavere viskositet har en tendens til at blande sig lettere end dem med højere viskositet.
- Meget viskøse væsker udviser langsommere molekylær diffusion og svagere intermolekylære interaktioner, hvilket hindrer blandingsprocessen.
6. Faseadskillelse:
- Afhængigt af arten af væskerne og deres vekselvirkninger, kan de udvise fuldstændig blanding (dannende en homogen opløsning), delvis blanding (dannende en emulsion) eller forblive ublandbare (adskilt i adskilte lag).
- Faktorer som temperatur, tryk og sammensætning kan påvirke væskernes faseadfærd.
Ved at udforske interaktioner på atomniveau, intermolekylære kræfter og molekylær dynamik, der er involveret i blanding af væsker, får forskere indsigt i en lang række fænomener, herunder væskestrømning, væske-væske-ekstraktion, formulering af emulsioner og legeringer og adfærden af flerfasede systemer. Disse forståelser har anvendelser inden for forskellige områder, såsom materialevidenskab, kemiteknik, farmaceutiske formuleringer og miljøvidenskab.
 Varme artikler
Varme artikler
-
 Ny elektronisk enhed registrerer eksplosive dampeKredit:National Research Nuclear University Forskere fra National Research Nuclear University MEPhI (Rusland) har præsenteret en detektor, der kan skelne lugte bedre end en servicehund. En lille e
Ny elektronisk enhed registrerer eksplosive dampeKredit:National Research Nuclear University Forskere fra National Research Nuclear University MEPhI (Rusland) har præsenteret en detektor, der kan skelne lugte bedre end en servicehund. En lille e -
 Artificial Chemist 2.0:Quantum dot R&D på mindre end en timeDette farvehjul af kvanteprikker fremhæver nogle af de farver, der kan laves med Artificial Chemist 2.0. Kredit:Milad Abolhasani, NC State University En ny teknologi, kaldet Artificial Chemist 2.0
Artificial Chemist 2.0:Quantum dot R&D på mindre end en timeDette farvehjul af kvanteprikker fremhæver nogle af de farver, der kan laves med Artificial Chemist 2.0. Kredit:Milad Abolhasani, NC State University En ny teknologi, kaldet Artificial Chemist 2.0 -
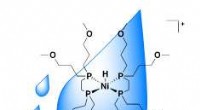 Ny nikkelkatalysator opererer i vand for at omdanne drivhusgas til kemisk råmaterialeNy nikkelkatalysator tilføjer hydrogen (H2) til kuldioxid (CO2) i vand ved hjælp af bikarbonat (NaHCO 3 ) som base. Propylethergrupperne på phosphinliganderne (lange kæder) gør nikkel (Ni)-katalysat
Ny nikkelkatalysator opererer i vand for at omdanne drivhusgas til kemisk råmaterialeNy nikkelkatalysator tilføjer hydrogen (H2) til kuldioxid (CO2) i vand ved hjælp af bikarbonat (NaHCO 3 ) som base. Propylethergrupperne på phosphinliganderne (lange kæder) gør nikkel (Ni)-katalysat -
 Ny forskning giver udvidet indsigt i hjernens reaktion på opioiderKredit:CC0 Public Domain Opioider er stærke smertestillende midler, der virker på hjernen, men de har en række skadelige bivirkninger, herunder afhængighed. Forskere fra Max Planck Institute of Bi
Ny forskning giver udvidet indsigt i hjernens reaktion på opioiderKredit:CC0 Public Domain Opioider er stærke smertestillende midler, der virker på hjernen, men de har en række skadelige bivirkninger, herunder afhængighed. Forskere fra Max Planck Institute of Bi
- Forskning viser, at insekter var den vigtigste fødekilde for millioner af år siden
- Det grønøjede monster:Hvordan at omfavne jalousi på arbejdet kan gøre dig mere produktiv
- Multi-messenger astronomi tilbyder nye estimater af neutronstjernestørrelse og universets udvidelse
- Cool Earth -teori kaster mere lys over diamanter
- Slående støj via superposition af ordre
- Slack Technologies stiger i Wall Street-debuten


