Hvordan adskiller en svag syre sig fra fortyndet syre?
1. Styrke:
- Svag syre:En svag syre er en syre, der kun delvist dissocierer i vand, hvilket betyder, at den ikke helt nedbrydes til sine ioner, når den opløses i vand. Som følge heraf er koncentrationen af hydrogenioner (H+) produceret af en svag syre relativt lav.
- Fortyndet syre:En fortyndet syre er en syre, der er blevet blandet med en stor mængde vand. Mens syren i sig selv kan være stærk (dvs. dissocierer fuldstændigt i vand), når den fortyndes, falder koncentrationen af hydrogenioner på grund af det øgede volumen af opløsningen.
2. pH:
- Svag syre:Svage syrer har en højere pH sammenlignet med stærke syrer af samme koncentration. Dette skyldes, at svage syrer producerer færre brintioner i vand, hvilket resulterer i et lavere surhedsniveau.
- Fortyndet syre:Fortyndede syrer har en højere pH sammenlignet med koncentrerede syrer af samme type. Når en syre fortyndes, falder hydrogenionkoncentrationen, hvilket fører til en højere pH-værdi.
3. Dissociation:
- Svag syre:Svage syrer gennemgår delvis dissociation, hvilket betyder, at kun en lille del af syremolekylerne nedbrydes til ioner i vand. Denne partielle dissociation resulterer i en lavere koncentration af hydrogenioner.
- Fortyndet syre:Fortyndede syrer undergår fuldstændig dissociation, ligesom koncentrerede syrer. Men på grund af det øgede volumen af vand er koncentrationen af hydrogenioner lavere i en fortyndet syre sammenlignet med en koncentreret syre af samme type.
4. Eksempler:
- Svage syrer:Nogle almindelige eksempler på svage syrer omfatter eddikesyre (eddike), kulsyre (til stede i kulsyreholdige drikkevarer) og flussyre.
- Fortyndede syrer:Fortyndede syrer kan fremstilles ved at blande enhver stærk syre med vand. For eksempel ville fortynding af saltsyre med vand skabe en fortyndet saltsyreopløsning.
Sammenfattende er en svag syre en syre, der delvist dissocierer i vand, hvilket resulterer i en lavere koncentration af hydrogenioner og en højere pH sammenlignet med stærke syrer. På den anden side er en fortyndet syre en syre, der er blevet blandet med vand, hvilket fører til en lavere koncentration af hydrogenioner sammenlignet med den koncentrerede form af den samme syre.
 Varme artikler
Varme artikler
-
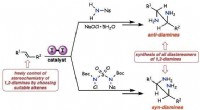 Molekylært jod katalyserer processer til antivirale og farmaceutiske synteserFigur 1. Skematisk diagram af anti- og syn-diamineringerne af alkener ved anvendelse af jodkatalysator. Kredit:Osaka University Syntetisering af lægemidler til kræft, virale sygdomme, og andre med
Molekylært jod katalyserer processer til antivirale og farmaceutiske synteserFigur 1. Skematisk diagram af anti- og syn-diamineringerne af alkener ved anvendelse af jodkatalysator. Kredit:Osaka University Syntetisering af lægemidler til kræft, virale sygdomme, og andre med -
 Ny metode til at opdage og visualisere sædceller genvundet fra retsmedicinsk bevisKredit:CC0 Public Domain En af de mest værdifulde former for retsmedicinsk bevismateriale i tilfælde af mandlige begåede seksuelle overgreb er tilstedeværelsen af sæd, enten i form af pletter ef
Ny metode til at opdage og visualisere sædceller genvundet fra retsmedicinsk bevisKredit:CC0 Public Domain En af de mest værdifulde former for retsmedicinsk bevismateriale i tilfælde af mandlige begåede seksuelle overgreb er tilstedeværelsen af sæd, enten i form af pletter ef -
 Ny forbindelse effektiv mod lægemiddelresistente patogener, kan føre til nye antibiotikaKredit:CC0 Public Domain Forskere fra North Carolina State University har syntetiseret en analog af lipoxazolidinon A, et lille molekyle, der er effektivt mod lægemiddelresistente bakterier som MR
Ny forbindelse effektiv mod lægemiddelresistente patogener, kan føre til nye antibiotikaKredit:CC0 Public Domain Forskere fra North Carolina State University har syntetiseret en analog af lipoxazolidinon A, et lille molekyle, der er effektivt mod lægemiddelresistente bakterier som MR -
 Nøglen er i belægningen:Flerlagsbelægning for at forbedre korrosionsbestandigheden af stålFlerlagsbelægningen har vist høj modstandsdygtighed over for rust og kan have vidtrækkende konsekvenser på byggeområdet. Kredit:Korea Maritime &Ocean University Stålets styrke gør det til et af de
Nøglen er i belægningen:Flerlagsbelægning for at forbedre korrosionsbestandigheden af stålFlerlagsbelægningen har vist høj modstandsdygtighed over for rust og kan have vidtrækkende konsekvenser på byggeområdet. Kredit:Korea Maritime &Ocean University Stålets styrke gør det til et af de
- Hvad var den største bølge nogensinde registreret?
- Hvad sker der med sproget, når befolkningerne vokser? Det forenkler, siger forskere
- Bud på miljørettighedspagt skal starte i Paris
- Indflydelsesrige elektroner? Fysikere afdækker et kvantforhold
- Ny måde at rense arrays af enkeltvæggede kulstof nanorør et skridt mod post-silicium kredsløb
- Cubanerne får tidlig smag af mobilt internet i systemtest


