Hvorfor har isotoper af det samme grundstof forskellige tætheder?
Massefylde er defineret som masse pr. volumenhed. Da isotoper har det samme antal protoner, vil de have et tilsvarende antal elektroner, der kredser om kernen. Det betyder, at atomets samlede ladning forbliver den samme. Men tilføjelsen af neutroner øger atomets masse uden at ændre dets størrelse væsentligt. Som et resultat vil isotoper med flere neutroner have en højere tæthed end isotoper med færre neutroner.
Overvej for eksempel kulstof-12 og kulstof-13. Kulstof-12 har 6 protoner, 6 neutroner og 6 elektroner, mens kulstof-13 har 6 protoner, 7 neutroner og 6 elektroner. Tilsætningen af en neutron øger massen af kulstof-13 med omkring 1,6%, men ændrer ikke dens størrelse væsentligt. Som et resultat er kulstof-13 tættere end kulstof-12.
Forskellen i tæthed mellem isotoper kan bruges til at adskille dem. Dette sker gennem en proces kaldet isotopseparation, som bruges i en række forskellige anvendelser, såsom produktion af nukleart brændsel og berigelse af uran til brug i atomreaktorer.
Sidste artikelKan du hælde husholdningssyrer som eddike ned i vasken?
Næste artikelHvorfor brænder natriumoxid og klorid den samme farve?
 Varme artikler
Varme artikler
-
 Løsningen på et forvirrende fænomen kan åbne døren til forbedret koldsprøjteeffektivitetDen øverste del viser en koldspray kobber belægning, med meget synlige hvirvellignende strukturer, der snurrer rundt om et aluminiumsunderlag i bunddelen. Kredit:EBSD Et internationalt forskerteam
Løsningen på et forvirrende fænomen kan åbne døren til forbedret koldsprøjteeffektivitetDen øverste del viser en koldspray kobber belægning, med meget synlige hvirvellignende strukturer, der snurrer rundt om et aluminiumsunderlag i bunddelen. Kredit:EBSD Et internationalt forskerteam -
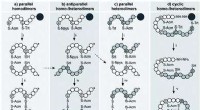 Bioinspirerede strategier til udvikling af nye lægemidlerFig. 1 Syntetiske strategier mod parallelle, antiparallelle og cykliske to-disulfidbindingshomo- og heterodimerer af VP/OT. Anvendte ortogonale beskyttelsesgrupper:Acm, acetamidomethyl; Npys, 3-nitro
Bioinspirerede strategier til udvikling af nye lægemidlerFig. 1 Syntetiske strategier mod parallelle, antiparallelle og cykliske to-disulfidbindingshomo- og heterodimerer af VP/OT. Anvendte ortogonale beskyttelsesgrupper:Acm, acetamidomethyl; Npys, 3-nitro -
 En luftstabil og vandtæt lithiummetalanodeDiagram over Li-wax-PEO og dens stabilitet i luft og vand. Kredit:Science China Press Lithiummetalanode tilbyder en lovende vej til at opgradere energitætheden af lithium-ion-batterier på grund
En luftstabil og vandtæt lithiummetalanodeDiagram over Li-wax-PEO og dens stabilitet i luft og vand. Kredit:Science China Press Lithiummetalanode tilbyder en lovende vej til at opgradere energitætheden af lithium-ion-batterier på grund -
 Forskere designer opgraderingsenhed til massespektrometreSkoltech og MIPT-forsker Yury Kostyukevich, en af skaberne af den nye enhed. Kredit:Skoltech Forskere fra Skoltech og MIPT har udviklet en enhed til at opgradere massespektrometre, der bruges ti
Forskere designer opgraderingsenhed til massespektrometreSkoltech og MIPT-forsker Yury Kostyukevich, en af skaberne af den nye enhed. Kredit:Skoltech Forskere fra Skoltech og MIPT har udviklet en enhed til at opgradere massespektrometre, der bruges ti
- Kvantenøglefordeling baseret på kvantesammenfiltring af høj kvalitet
- Forskere undersøger træk ved stjernehobe omkring supermassive sorte huller
- Hvorfor det fjerne Antarktis er så vigtigt i en opvarmende verden
- Astronomer opdager en klasse af mærkelige objekter nær vores galaksers enorme sorte hul
- Hvordan fungerer vacciner med immunsystemet?
- Sikre metropolitiske kvantenetværk bevæger sig et skridt nærmere


