Hvilken primær standard bruges til at titrere mod saltsyre?
Na2CO3(aq) + 2HCl(aq) → 2NaCl(aq) + H2O(l) + CO2(g)
Da natriumcarbonat er en primær standard, bruges den i vid udstrækning til nøjagtig bestemmelse af koncentrationen af HCl-opløsninger. For at udføre titreringen vejes en kendt masse natriumcarbonat nøjagtigt og opløses i vand. Den resulterende opløsning tilsættes derefter langsomt til HCI-opløsningen under konstant omrøring, indtil slutpunktet er nået.
Slutpunktet for titreringen bestemmes ved hjælp af en indikator, som skifter farve som reaktion på pH-ændringen. En almindeligt anvendt indikator for titrering af HCl med natriumcarbonat er methylorange, som skifter fra rød til gul, når pH-værdien af opløsningen stiger. Ækvivalenspunktet nås, når mængden af tilsat natriumcarbonat er støkiometrisk ækvivalent med mængden af HCl til stede i opløsningen.
Ved omhyggeligt at registrere mængden af HCl, der kræves for at nå ækvivalenspunktet, kan den nøjagtige koncentration af HCl-opløsningen beregnes nøjagtigt. Denne titreringsmetode er pålidelig, præcis og kan give nøjagtige resultater til bestemmelse af koncentrationen af HCl-opløsninger i forskellige analytiske og laboratorieindstillinger.
Sidste artikelHvad er PH og ledningsevne i DM-vand?
Næste artikelEr homogene blandingspartikler spredt jævnt?
 Varme artikler
Varme artikler
-
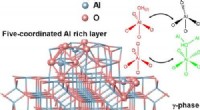 Karten af fem-koordineret aluminium på γ-Al2O3 overfladeGrafisk abstrakt. Kredit:ACS Central Science (2022). DOI:10.1021/acscentsci.1c01497 y-Al2 O3 , en vigtig katalysator og katalysatorbærer, er meget udbredt i forskellige industrielle anvendelser. De
Karten af fem-koordineret aluminium på γ-Al2O3 overfladeGrafisk abstrakt. Kredit:ACS Central Science (2022). DOI:10.1021/acscentsci.1c01497 y-Al2 O3 , en vigtig katalysator og katalysatorbærer, er meget udbredt i forskellige industrielle anvendelser. De -
 Anvendelse af beregningskemi til at simulere realistiske kemiske processerKredit:University of California - San Diego Videnskabens vand er mudret i disse dage - især ved University of California San Diego, hvor alt, der adskiller en kemiker fra en fysiker, i nogle tilfæ
Anvendelse af beregningskemi til at simulere realistiske kemiske processerKredit:University of California - San Diego Videnskabens vand er mudret i disse dage - især ved University of California San Diego, hvor alt, der adskiller en kemiker fra en fysiker, i nogle tilfæ -
 Find de faktorer, der påvirker stålkorrosionen mest i armeret beton mestMercedes Sánchez, undersøgelse af undersøgelsen. Kredit:Universidad de Córdoba Siden de egyptiske pyramider og det romerske Colosseum blev bygget, menneskeheden har ledt efter en overkommelig pris
Find de faktorer, der påvirker stålkorrosionen mest i armeret beton mestMercedes Sánchez, undersøgelse af undersøgelsen. Kredit:Universidad de Córdoba Siden de egyptiske pyramider og det romerske Colosseum blev bygget, menneskeheden har ledt efter en overkommelig pris -
 Flydende retsmedicin kan føre til mere sikkert drikkevandInstrumentet er designet til at analysere kvaliteten af væsker ved hjælp af den fotoakustiske effekt, eller dannelse af lydbølger efter lys er absorberet i et materiale. MU -forskerne mener, at dett
Flydende retsmedicin kan føre til mere sikkert drikkevandInstrumentet er designet til at analysere kvaliteten af væsker ved hjælp af den fotoakustiske effekt, eller dannelse af lydbølger efter lys er absorberet i et materiale. MU -forskerne mener, at dett


