Brug Lewis-strukturer og vsepr-teori til at bestemme hvilke ch4 ch3cl der er polære ikke-polære?
* Lewis struktur:H-C-H
* VSEPR form:tetraedrisk
* Polaritet:ikke-polær
CH3Cl
* Lewis struktur:H-C-Cl
* VSEPR form:tetraedrisk
* Polaritet:polær
Forklaring:
I CH4 er de fire hydrogenatomer arrangeret symmetrisk omkring carbonatomet. Det betyder, at brintatomernes elektronegativitet ophæves, og molekylet er upolært.
I CH3Cl er chloratomet mere elektronegativt end hydrogenatomerne. Det betyder, at elektronerne i C-Cl-bindingen trækkes mod kloratomet, hvilket skaber en polær binding. Molekylet som helhed er også polært, fordi den positive ende af C-Cl-bindingen er tættere på kloratomet end den negative ende.
Sidste artikelEr vand eller aluminium en bedre leder?
Næste artikelEr aluminiumoxid metal eller ikke-metal?
 Varme artikler
Varme artikler
-
 Udvikling af en ny billig galliumnitrid (GaN) krystalfremstillingsenhedUdseende af THVPE krystalvækstovn. Kredit:Taiyo Nippon Sanso Co. JST annoncerer den succesrige udvikling af en højkvalitets bulk GaN vækstenhed baseret på THVPE-metoden, et udviklingsemne for det
Udvikling af en ny billig galliumnitrid (GaN) krystalfremstillingsenhedUdseende af THVPE krystalvækstovn. Kredit:Taiyo Nippon Sanso Co. JST annoncerer den succesrige udvikling af en højkvalitets bulk GaN vækstenhed baseret på THVPE-metoden, et udviklingsemne for det -
 Forbedret forståelse af industrielle elektrodeprocesserElektroden, der bruges til målingerne, er kun en hundrededel i tykkelsen af et menneskehår. Kredit:RUB, Marquard I den industrielle produktion af klor, specielle elektroder er for nylig blevet i
Forbedret forståelse af industrielle elektrodeprocesserElektroden, der bruges til målingerne, er kun en hundrededel i tykkelsen af et menneskehår. Kredit:RUB, Marquard I den industrielle produktion af klor, specielle elektroder er for nylig blevet i -
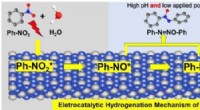 Hydrogeneringsregulering af nitrobenzen i elektrokatalytiske processer realiseretGrafisk abstrakt. En omfattende forståelse af selektiviteten over for elektrokatalytiske hydrogeneringsprodukter af nitrobenzen blev udført eksperimentelt og teoretisk over en Cu3Pt/C -legeringskataly
Hydrogeneringsregulering af nitrobenzen i elektrokatalytiske processer realiseretGrafisk abstrakt. En omfattende forståelse af selektiviteten over for elektrokatalytiske hydrogeneringsprodukter af nitrobenzen blev udført eksperimentelt og teoretisk over en Cu3Pt/C -legeringskataly -
 Forskere afdækker mekanismen for svampeluminescens og skaber selvlysende gærSelvlysende gær. Kredit:Sergey Shakhov Russiske forskere med kolleger fra Storbritannien, Spanien, Brasilien, Japan og Østrig har fuldt ud beskrevet mekanismen for svampeluminescens. De rapportere
Forskere afdækker mekanismen for svampeluminescens og skaber selvlysende gærSelvlysende gær. Kredit:Sergey Shakhov Russiske forskere med kolleger fra Storbritannien, Spanien, Brasilien, Japan og Østrig har fuldt ud beskrevet mekanismen for svampeluminescens. De rapportere
- Gratis datasætarkiv hjælper forskere med hurtigt at finde en nål i en høstak
- Paradokset ved en frielektronlaser uden laseren
- Fra aske til advarsler:Videnskab hjælper med at beskytte Colorado-rejsende
- Nanoribbons til grafen -transistorer
- Sony, Amazon, andre dropper ud af det store teknologishow på grund af virus
- Hvorfor er forfaldsbakterier afgørende for livet på jorden?


