Hvad er molariteten af opløsningen opnået, når 26,3 g kaliumbromid fortyndes til 487 ml?
```
Molaritet (M) =mol opløst stof / liter opløsning
```
Først skal vi beregne mol kaliumbromid (KBr) opløst i opløsningen:
```
Mol af KBr =masse af KBr / molær masse af KBr
```
Den molære masse af KBr er cirka 119,0 g/mol.
```
Mol KBr =26,3 g / 119,0 g/mol =0,221 mol
```
Dernæst skal vi konvertere opløsningens volumen fra milliliter (mL) til liter (L):
```
Opløsningsvolumen =487 ml =0,487 L
```
Nu kan vi beregne molariteten af opløsningen:
```
Molaritet (M) =0,221 mol / 0,487 L =0,454 M
```
Derfor er molariteten af opløsningen opnået, når 26,3 g kaliumbromid fortyndes til 487 ml, 0,454 M.
 Varme artikler
Varme artikler
-
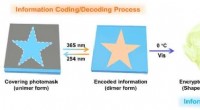 Ny fluorescerende organohydrogel foreslået for at opnå dobbelt informationskrypteringInformationskodning/dekodning og kryptering/dekryptering baseret på den fluorescerende organohydrogel. Kredit:NIMTE Smart Polymer Materials Group ledet af prof. Chen Tao ved Ningbo Institute of Mat
Ny fluorescerende organohydrogel foreslået for at opnå dobbelt informationskrypteringInformationskodning/dekodning og kryptering/dekryptering baseret på den fluorescerende organohydrogel. Kredit:NIMTE Smart Polymer Materials Group ledet af prof. Chen Tao ved Ningbo Institute of Mat -
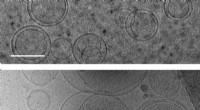 De første celler kan være opstået, fordi byggesten af proteiner stabiliserede membranerBilleder af membraner (cirkler) taget ved hjælp af transmissionselektronkryomikroskopi. Øverst:membraner i en opløsning, der ikke indeholder aminosyrer. Nederst:membraner i en opløsning indeholdende s
De første celler kan være opstået, fordi byggesten af proteiner stabiliserede membranerBilleder af membraner (cirkler) taget ved hjælp af transmissionselektronkryomikroskopi. Øverst:membraner i en opløsning, der ikke indeholder aminosyrer. Nederst:membraner i en opløsning indeholdende s -
 Brug af bakterier til at fremskynde CO2-opsamling i haveneBerkeley Lab-forsker Peter Agbo blev tildelt en bevilling til et kulstoffangstprojekt under Labs Carbon Negative Initiative. Kredit:Marilyn Sargent/Berkeley Lab Du er måske bekendt med direkte luft
Brug af bakterier til at fremskynde CO2-opsamling i haveneBerkeley Lab-forsker Peter Agbo blev tildelt en bevilling til et kulstoffangstprojekt under Labs Carbon Negative Initiative. Kredit:Marilyn Sargent/Berkeley Lab Du er måske bekendt med direkte luft -
 Styrkelse af passiv prøveudtagning af upolare kemikalierPassiv prøveudtager. Kredit:Ian Allan Passiv prøveudtagning er en værdifuld teknik til overvågning af koncentrationsniveauer af hydrofobe persistente organiske forurenende stoffer (POPer) i havmil
Styrkelse af passiv prøveudtagning af upolare kemikalierPassiv prøveudtager. Kredit:Ian Allan Passiv prøveudtagning er en værdifuld teknik til overvågning af koncentrationsniveauer af hydrofobe persistente organiske forurenende stoffer (POPer) i havmil
- Robotisk grebsmekanisme efterligner, hvordan søanemoner fanger bytte
- Sporing og bekæmpelse af brande på jorden og udenfor
- Liste over metaller, der tiltrækkes af magneter
- Opbygning af et billede af fædre i familiens retssystem i England
- Egg Drop Device Ideas
- Astronomer undersøger den kemiske sammensætning af en nærliggende stjernedannende dværggalakse


