Hvad er den elektrode, hvor klor dannes?
Under elektrolyse føres en jævnstrøm gennem saltvandsopløsningen, hvilket får de positivt ladede natriumioner (Na+) til at migrere mod katoden (negativ elektrode) og de negativt ladede chloridioner (Cl-) til at migrere mod anoden (positiv elektrode). ).
Ved katoden får natriumionerne elektroner og bliver til neutrale natriumatomer, som derefter reagerer med vandmolekyler og danner brintgas (H2) og natriumhydroxid (NaOH).
Ved anoden mister chloridionerne elektroner og bliver til klorgas (Cl2). Klorgassen bobler op og kan opsamles.
Den overordnede reaktion for elektrolyse af saltlage er:
NaCl(aq) + H2O(l) → Cl2(g) + H2(g) + NaOH(aq)
Sidste artikelHvad er bi2SbTe3?
Næste artikelHvilken fysisk og kemisk ændring sker, når der kommer LPG ud af cylinderen forbrændinger?
 Varme artikler
Varme artikler
-
 Indesluttet magnetisk kolloidt system til kontrollerbar væsketransportSkema af indesluttede kolloider i forskellige tilstande via fjern og dynamisk magnetisk regulering Kredit:Science China Press Kolloide suspensioner af mikroskopiske partikler viser kompleks og int
Indesluttet magnetisk kolloidt system til kontrollerbar væsketransportSkema af indesluttede kolloider i forskellige tilstande via fjern og dynamisk magnetisk regulering Kredit:Science China Press Kolloide suspensioner af mikroskopiske partikler viser kompleks og int -
 Forskere afslører cryo-elektronmikroskopistruktur af et herpesvirus capsid ved 3,1 ÅngstrømOversigt over interaktionerne på den indre kapsidoverflade. Kredit:WANG Xiangxi Herpesvirus er genetisk og strukturelt en af de mest komplekse vira. Det spredes effektivt i værtspopulationen, fo
Forskere afslører cryo-elektronmikroskopistruktur af et herpesvirus capsid ved 3,1 ÅngstrømOversigt over interaktionerne på den indre kapsidoverflade. Kredit:WANG Xiangxi Herpesvirus er genetisk og strukturelt en af de mest komplekse vira. Det spredes effektivt i værtspopulationen, fo -
 Forlænger levetiden for polymerelektrolytbrændselsceller med en nanodisperseret ionomerSkema af Nafion-ionomerer på katalysatoroverfladerne. (A) Fordeling af konventionelle ionomerer syntetiseret ved emulsionspolymerisation. (B) Fordeling af laboratoriefremstillede ionomerer syntetisere
Forlænger levetiden for polymerelektrolytbrændselsceller med en nanodisperseret ionomerSkema af Nafion-ionomerer på katalysatoroverfladerne. (A) Fordeling af konventionelle ionomerer syntetiseret ved emulsionspolymerisation. (B) Fordeling af laboratoriefremstillede ionomerer syntetisere -
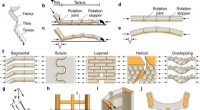 Ny opdagelse i dyreeksoskeletter fører til fremskridt inden for design af byggematerialerSegmentmotiv inspireret af strukturen af leddyrets eksoskelet. Kredit:Nature Communications (2022). DOI:10.1038/s41467-022-28991-5 Forskere fra Monash University har opdaget et nyt designmotiv af
Ny opdagelse i dyreeksoskeletter fører til fremskridt inden for design af byggematerialerSegmentmotiv inspireret af strukturen af leddyrets eksoskelet. Kredit:Nature Communications (2022). DOI:10.1038/s41467-022-28991-5 Forskere fra Monash University har opdaget et nyt designmotiv af
- Hvad gør Netflix, Har Google og planetsystemer til fælles?
- Sådan finder du området af en rektangulær prism
- Avanceret eksperimentel opsætning udvider jagten på skjulte partikler af mørkt stof
- Facebook ud over Facebook? Instagram, Messenger rykker op
- Grundlæggende og fotodetektoranvendelse af van der Waals Schottky-kryds
- Hvorfor er heliumgas kemisk inaktiv?


