Når en elektron sendes til acceptormolekyle såsom NADP, hvad sker der NADP?
1. NADP+-reduktion:I starten eksisterer NADP i sin oxiderede form, forkortet NADP+. Når den accepterer en elektron, reduceres den til NADPH.
2. Forstærkning af hydridion (H-):Tilføjelsen af en elektron til NADP+ er ledsaget af overførslen af en hydrogenion (H+) og to elektroner. En af elektronerne bruges til at reducere det positivt ladede nitrogenatom i nikotinamidringen, mens den anden elektron sammen med hydrogenionen danner en hydridion (H-).
3. Dannelse af NADPH:Den reducerede form af NADP, nu kendt som NADPH, bærer den nyligt erhvervede hydridion (H-) og har en negativ ladning.
Den overordnede reaktion kan repræsenteres som:
NADP+ + 2e- + H+ → NADPH + H+
Sammenfattende, når en elektron sendes til NADP, bliver den reduceret til NADPH, får en hydridion (H-) og undergår en ændring i dens oxidationstilstand. NADPH fungerer derefter som en bærer af reducerende ækvivalenter (elektroner og hydrogenioner) i forskellige biokemiske reaktioner.
 Varme artikler
Varme artikler
-
 Forskere opretter vandfiltreringsmembraner, der kan rense sig selvEn kunstners gengivelse af lysinduceret selvrensning af en forurenet membran. Kredit:Argonne National Laboratory Forskere ved Department of Energys (DOE) Argonne National Laboratory har udviklet e
Forskere opretter vandfiltreringsmembraner, der kan rense sig selvEn kunstners gengivelse af lysinduceret selvrensning af en forurenet membran. Kredit:Argonne National Laboratory Forskere ved Department of Energys (DOE) Argonne National Laboratory har udviklet e -
 Undersøisk liv lover at dræbe tuberkuloseDr. Rohde og hans team arbejder på at afdække hemmelighederne bag svampe og andet undersøisk liv, der kan hjælpe med at bekæmpe tuberkulose. Kredit:University of Central Florida Et team af forsker
Undersøisk liv lover at dræbe tuberkuloseDr. Rohde og hans team arbejder på at afdække hemmelighederne bag svampe og andet undersøisk liv, der kan hjælpe med at bekæmpe tuberkulose. Kredit:University of Central Florida Et team af forsker -
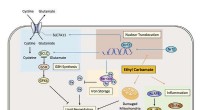 Forskere opdager mekanismen for ethylcarbamat-induceret toksicitet i fermenteret madKredit:Redox Biology Ethylcarbamat (EC) er et farligt stof, der naturligt produceres under gæringen af fødevarer og drikkevarer. Det er blevet kategoriseret som sandsynligvis kræftfremkaldende f
Forskere opdager mekanismen for ethylcarbamat-induceret toksicitet i fermenteret madKredit:Redox Biology Ethylcarbamat (EC) er et farligt stof, der naturligt produceres under gæringen af fødevarer og drikkevarer. Det er blevet kategoriseret som sandsynligvis kræftfremkaldende f -
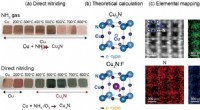 Højtydende nitrid-halvleder til miljøvenlig solcelle(a) Dette er et kobber- og kobbernitrid. (b) Teoretisk beregning for P-type og N-type kobbernitrid. (c) Direkte observation af fluorposition i fluordoteret kobbernitrid.(a) Et billede af tyndfilms kob
Højtydende nitrid-halvleder til miljøvenlig solcelle(a) Dette er et kobber- og kobbernitrid. (b) Teoretisk beregning for P-type og N-type kobbernitrid. (c) Direkte observation af fluorposition i fluordoteret kobbernitrid.(a) Et billede af tyndfilms kob
- Små organismer med massiv påvirkning
- Regnskovsvenlige levebrød kan være mere lukrative end guldminedrift
- Sådan konverteres område af en cirkel til Square Feet
- Forudsagt eksperimentel test vil afklare, hvordan lys interagerer med stof ved høje energier
- TESS leverer ny indsigt i en ultrahot verden
- Hvordan kyllinger blev det ultimative symbol på antropocæn


