Hvor mange atomer er der i 18g C6H12O6?
1. Beregn molmassen af C6H12O6:
- C6H12O6 =(6 × 12,01 g/mol C) + (12 × 1,01 g/mol H) + (6 × 16,00 g/mol O)
- Molær masse =180,16 g/mol
2. Konverter den givne masse (18 g) til mol:
- Mol af C6H12O6 =18 g / 180,16 g/mol
- Mol C6H12O6 =0,1 mol
3. Brug Avogadros tal til at beregne antallet af atomer:
- Antal molekyler i 0,1 mol =0,1 mol × 6,022 × 10^23 molekyler/mol
- Antal molekyler =6,022 × 10^22 molekyler
4. Bestem det samlede antal atomer i et enkelt molekyle af C6H12O6:
- C6H12O6 indeholder 6 carbonatomer, 12 hydrogenatomer og 6 oxygenatomer.
- Totale atomer =6 C + 12 H + 6 O =24 atomer
5. Gang antallet af atomer pr. molekyle med antallet af molekyler:
- Samlet antal atomer i 18 g C6H12O6 =24 atomer/molekyle × 6,022 × 10^22 molekyler
- Samlede atomer =1,445 × 10^24 atomer
Derfor er der cirka 1,445 × 10^24 atomer til stede i 18 g C6H12O6.
 Varme artikler
Varme artikler
-
 Hæmmer eller fremmer zink vækst af nyresten? Godt, beggeKredit:CC0 Public Domain Der skete en sjov ting på vejen til at opdage, hvordan zink påvirker nyresten - to forskellige teorier dukkede op, hver modsiger hinanden. Et:Zink stopper væksten af de
Hæmmer eller fremmer zink vækst af nyresten? Godt, beggeKredit:CC0 Public Domain Der skete en sjov ting på vejen til at opdage, hvordan zink påvirker nyresten - to forskellige teorier dukkede op, hver modsiger hinanden. Et:Zink stopper væksten af de -
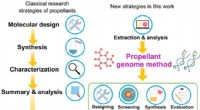 Design af højtydende hypergoliske drivmidler til rumraketter baseret på materialernes genomNy strategi i design af drivmiddel baseret på genommetoden. Kredit:Science Advances, doi:10.1126/sciadv.abb1899 En ny generation af raketdrivmidler til udforskning af det dybe rum, såsom ioniske f
Design af højtydende hypergoliske drivmidler til rumraketter baseret på materialernes genomNy strategi i design af drivmiddel baseret på genommetoden. Kredit:Science Advances, doi:10.1126/sciadv.abb1899 En ny generation af raketdrivmidler til udforskning af det dybe rum, såsom ioniske f -
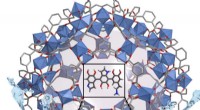 Fjernelse af tungmetaller fra vand med MOF'erEn organisk metalramme kan fjerne bly fra vandprøver, få dem til EPA-godkendte niveauer på få sekunder. Kredit:American Chemical Society Det anslås, at 1 milliard mennesker ikke har adgang til ren
Fjernelse af tungmetaller fra vand med MOF'erEn organisk metalramme kan fjerne bly fra vandprøver, få dem til EPA-godkendte niveauer på få sekunder. Kredit:American Chemical Society Det anslås, at 1 milliard mennesker ikke har adgang til ren -
 En billig organisk dampgenerator til at rense vandVarmen fra solen fordamper vandet, mens salt og andre materialer forbliver tilbage. Kredit:Thor Balkhed Det er blevet anslået, at en fjerdedel af verdens børn i 2040 vil bo i regioner, hvor der ma
En billig organisk dampgenerator til at rense vandVarmen fra solen fordamper vandet, mens salt og andre materialer forbliver tilbage. Kredit:Thor Balkhed Det er blevet anslået, at en fjerdedel af verdens børn i 2040 vil bo i regioner, hvor der ma
- Er det permanent kemisk forandring at tage et billede?
- Pandoravirus:Det smeltende Arktis frigiver ældgamle bakterier – hvor bekymrede skal vi være?
- Tyngdekraftseksperimenter på køkkenbordet:Hvorfor en lille bitte måling kan være et stort spring…
- Japans anklagere søger at forlænge Ghosn -tilbageholdelsen
- Sådan fungerer miljøterrorisme
- Stærkt skælv rammer Solomons; nogle skader, men ingen tsunami


