Er der større sandsynlighed for, at et diatomisk molekyle holdes sammen af en kovalent binding eller en ionisk og hvorfor?
Derudover skal elektronegativiteten af de to atomer i et diatomisk molekyle være ens, for at der kan dannes en kovalent binding. Elektronegativitet er et mål for, hvor stærkt et atom tiltrækker elektroner. Hvis elektronegativiteten af de to atomer er for forskellig, vil det ene atom tiltrække elektronerne stærkere end det andet, og det vil resultere i en ionbinding.
For eksempel holdes det diatomiske molekyle hydrogenchlorid (HCl) sammen af en kovalent binding, fordi elektronegativiteten af hydrogen og klor er ens. I modsætning hertil holdes den ioniske forbindelse natriumchlorid (NaCl) sammen af en ionbinding, fordi elektronegativiteten af natrium og klor er meget forskellig.
Sidste artikelHvordan udvindes tin fra sin malm?
Næste artikelHvad er karakteristika ved grundstoffer og forbindelser?
 Varme artikler
Varme artikler
-
 Fingeraftryks-narkotest virker på levende og afdødeKredit:CC0 Public Domain En revolutionerende lægemiddeltest udviklet fra forskning udført ved University of East Anglia kan påvise fire klasser af lægemidler i spor af sved fundet i et fingeraftry
Fingeraftryks-narkotest virker på levende og afdødeKredit:CC0 Public Domain En revolutionerende lægemiddeltest udviklet fra forskning udført ved University of East Anglia kan påvise fire klasser af lægemidler i spor af sved fundet i et fingeraftry -
 Bygning fra gamle bygninger:Nedrivningsaffald bliver til ny betonDet franske firma Keey Aerogel kan producere sin aerogel-varmeisolering til omkring halvdelen af prisen ved at udvinde silica fra affaldsbeton i stedet for at bruge ny silica. Kredit:Keey Aerogel
Bygning fra gamle bygninger:Nedrivningsaffald bliver til ny betonDet franske firma Keey Aerogel kan producere sin aerogel-varmeisolering til omkring halvdelen af prisen ved at udvinde silica fra affaldsbeton i stedet for at bruge ny silica. Kredit:Keey Aerogel -
 Fuld af varm luft og stolt over det:Forbedring af gaslagring med MOF'erIdealiseret interpenetreret MOF -struktur. Den sammenfiltrede MOF kan sprede varme omtrent to gange hurtigere, end de bestanddele MOF kan separat, muligvis muliggør mere effektiv gaslagring. Kredit:Sw
Fuld af varm luft og stolt over det:Forbedring af gaslagring med MOF'erIdealiseret interpenetreret MOF -struktur. Den sammenfiltrede MOF kan sprede varme omtrent to gange hurtigere, end de bestanddele MOF kan separat, muligvis muliggør mere effektiv gaslagring. Kredit:Sw -
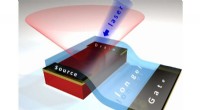 Lys fra en eksotisk krystalhalvleder kan føre til bedre solcellerKonceptuelt billede af en transistorenhed, der styrer fotoluminescens (den lyserøde kegle), der udsendes af en hybrid perovskitkrystal (den røde boks), der exciteres af en blå laserstråle, efter at sp
Lys fra en eksotisk krystalhalvleder kan føre til bedre solcellerKonceptuelt billede af en transistorenhed, der styrer fotoluminescens (den lyserøde kegle), der udsendes af en hybrid perovskitkrystal (den røde boks), der exciteres af en blå laserstråle, efter at sp
- Sentinel-2 fanger koralblegning af Great Barrier Reef
- Nye fluorescerende nanovesikler til intracellulær biomarkørdetektion
- Canberra-hedebølgen slår rekorder midt i truslen om skovbrand
- Britiske lovgivere:Vilde Vestens kryptovalutaer har brug for regulering
- Mættelige plasmoniske metaoverflader til låsning af lasertilstand
- Hvordan påvirker linsens tykkelse brændvidden?


