Hvad gør salpetersyre til en syre?
Når salpetersyre opløses i vand, gennemgår den ionisering, hvor bindingen mellem brint (H) og nitrogen (N) atomer bryder, og frigiver H+ ioner i opløsningen.
HNO3 + H2O ⇌ H3O+ + NO3-
I denne ligning er HNO3 syren, H2O er vand, H3O+ repræsenterer hydroniumionen (dannet når H+ kombineres med vand), og NO3- er nitrationen. H+-ionerne solvaterer med vandmolekyler og danner hydroniumioner, som bidrager til opløsningens sure egenskaber.
Koncentrationen af H+ ioner i en opløsning bestemmer dens surhedsgrad. Jo flere H+ ioner til stede, jo stærkere er syren. Salpetersyre er en stærk syre, fordi den dissocierer fuldstændigt i vand og frigiver næsten alle dens H+ ioner. Som et resultat har salpetersyreopløsninger en høj koncentration af H3O+ ioner og udviser stærke sure egenskaber.
Denne sure natur af salpetersyre opstår fra den polære natur af N-O-bindingerne og elektronegativiteten af oxygenatomer. Oxygenatomerne i nitrationen (-NO3) tiltrækker kraftigt elektroner fra hydrogenatomet, hvilket letter brydningen af O-H-bindingen og frigivelsen af H+-ioner.
Sidste artikelHvilken udvinding af salt fra havvand?
Næste artikelHvorfor er fosforsyre en svag syre?
 Varme artikler
Varme artikler
-
 Forskere udvikler et cellulosebiosensormateriale til avanceret vævsteknologiEn 3D-rekonstruktion af en cellulosematrix farvet med en pH-følsom biosensor. Kredit:Dr. R. Dmitriev I.M. Sechenov fra First Moscow State Medical University gik sammen med irske kolleger for at ud
Forskere udvikler et cellulosebiosensormateriale til avanceret vævsteknologiEn 3D-rekonstruktion af en cellulosematrix farvet med en pH-følsom biosensor. Kredit:Dr. R. Dmitriev I.M. Sechenov fra First Moscow State Medical University gik sammen med irske kolleger for at ud -
 Ny forskning finder manglende forbindelse mellem blød overfladeadhæsion og overfladeruhedAt forstå ruhed på sådanne mikroskopiske niveauer tillod forskere at forstå mekanikken i, hvordan bløde overflader klæber til dem. Kredit:University of Akron College of Polymer Science og Polymer Engi
Ny forskning finder manglende forbindelse mellem blød overfladeadhæsion og overfladeruhedAt forstå ruhed på sådanne mikroskopiske niveauer tillod forskere at forstå mekanikken i, hvordan bløde overflader klæber til dem. Kredit:University of Akron College of Polymer Science og Polymer Engi -
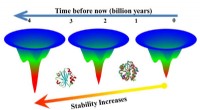 Proteiner, der kan tage varmenGamle proteiner kan tilbyde spor om konstruktionsproteiner til at modstå høje temperaturer, der kræves i industrielle applikationer. Kredit:Rensselaer Polytechnic Institute Gamle proteiner kan giv
Proteiner, der kan tage varmenGamle proteiner kan tilbyde spor om konstruktionsproteiner til at modstå høje temperaturer, der kræves i industrielle applikationer. Kredit:Rensselaer Polytechnic Institute Gamle proteiner kan giv -
 Kuldioxidmineralisering i geologisk almindelige bjergarter til kulstoflagringDen røde farve angiver, at sandsynligheden for forekomst af valenselektroner er 100 procent, den blå farve betyder, at der ikke findes elektroner i området, og den grønne farve betyder fri elektrongas
Kuldioxidmineralisering i geologisk almindelige bjergarter til kulstoflagringDen røde farve angiver, at sandsynligheden for forekomst af valenselektroner er 100 procent, den blå farve betyder, at der ikke findes elektroner i området, og den grønne farve betyder fri elektrongas
- Afdækning af fragmenteringsforskelle i chirale biomolekyler
- Verden skal handle for at dæmme op for bølgen af forurenende affald, advarer FN
- Kombinerer sollys og spildevandsnitrat for at gøre verdens nummer 2 kemikalie
- Sådan bestemmes astrologisk den bedste dag til at tage en prøve
- Sådan kører du en lightbulb Brug en Potato
- Ny nanopartikel retter sig mod tumorinfiltrerende immunceller, vipper kontakten


