Hvad skete der, da du blandede 3,0 ml AgNO3 og K2CO4 i reagensglasset?
2AgNO3 (aq) + K2CO3 (aq) --> Ag2CO3 (s) + 2KNO3 (aq)
Her er, hvad du ville observere, når du blander disse to løsninger:
1. Dannelse af bundfald: Så snart opløsningerne er blandet, vil du bemærke dannelsen af et hvidt bundfald. Dette bundfald er sølvcarbonat (Ag2CO3), som er uopløseligt i vand. Bundfaldet fremstår som en uklar suspension i reagensglasset.
2. Farveændring: Til at begynde med er AgNO3-opløsningen farveløs, og K2CO3-opløsningen kan også være farveløs eller let basisk (afhængig af dens koncentration). Efter blanding bliver opløsningen mælkehvid på grund af det suspenderede bundfald af Ag2CO3.
3. Opbrusning: Under reaktionen kan du observere noget brus eller bobler i reagensglasset. Dette er forårsaget af frigivelsen af kuldioxidgas (CO2). Reaktionen mellem carbonationer (CO3^2-) fra K2CO3 og sølvioner (Ag+) fra AgNO3 producerer CO2-gas som et biprodukt.
4. Udfældning af bundfald: Over tid vil bundfaldet af Ag2CO3 bundfælde sig i bunden af reagensglasset og efterlade en klar supernatantvæske over det. Supernatanten indeholder det opløselige produkt, kaliumnitrat (KNO3), som dannes under reaktionen.
5. Bekræftelse af udfældning: For at bekræfte dannelsen af Ag2CO3-udfældning kan du udføre yderligere tests. For eksempel kan du tilsætte et par dråber fortyndet salpetersyre (HNO3) til reagensglasset. Bundfaldet skal opløses i salpetersyre, hvilket indikerer, at det er sølvcarbonat.
 Varme artikler
Varme artikler
-
 Diagnosticering af kunst acne i Georgia OKeeffes malerierKig tæt på et detaljeret afsnit af Pedernal viser fremspring i mikronstørrelse fra metalsæber.Georgia OKeeffe. Pedernal, 1941. Olie på lærred, 19 x 30 1/4 tommer. Georgia OKeeffe Museum. Gave fra Geor
Diagnosticering af kunst acne i Georgia OKeeffes malerierKig tæt på et detaljeret afsnit af Pedernal viser fremspring i mikronstørrelse fra metalsæber.Georgia OKeeffe. Pedernal, 1941. Olie på lærred, 19 x 30 1/4 tommer. Georgia OKeeffe Museum. Gave fra Geor -
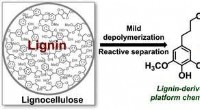 Gør træ til farmaceutiske ingredienserKredit:American Chemical Society Produktion af farligt affald under lægemiddelfremstilling er en alvorlig bekymring for medicinalindustrien. Typisk, store mængder brandfarlige opløsningsmidler anv
Gør træ til farmaceutiske ingredienserKredit:American Chemical Society Produktion af farligt affald under lægemiddelfremstilling er en alvorlig bekymring for medicinalindustrien. Typisk, store mængder brandfarlige opløsningsmidler anv -
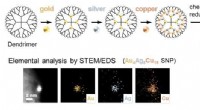 Sub-nanopartikelkatalysatorer fremstillet af møntelementer som effektive katalysatorerSkabelonsyntesen af møntmetallegerede SNPer ved hjælp af atomhybridiseringsmetoden. Tre metalelementer (guld, sølv, kobber) blandes her i en SNP på en en-nanometer skala. Kredit:Tokyo Institute of T
Sub-nanopartikelkatalysatorer fremstillet af møntelementer som effektive katalysatorerSkabelonsyntesen af møntmetallegerede SNPer ved hjælp af atomhybridiseringsmetoden. Tre metalelementer (guld, sølv, kobber) blandes her i en SNP på en en-nanometer skala. Kredit:Tokyo Institute of T -
 Uber medicin levering til kræftpatienterPh.d.-kandidaterne Samantha Wade og Sepehr Talebian, Dr Javad Foroughi, Fornemme professor Gordon Wallace og Dr. Kara Vine-Perrow. Kredit:Alex Pike Kræft er fortsat en af de største dødsårsager
Uber medicin levering til kræftpatienterPh.d.-kandidaterne Samantha Wade og Sepehr Talebian, Dr Javad Foroughi, Fornemme professor Gordon Wallace og Dr. Kara Vine-Perrow. Kredit:Alex Pike Kræft er fortsat en af de største dødsårsager
- En kødfri kost overalt vil ikke løse klimakrisen
- Hvorfor er folks hjerner forskellige størrelser?
- Oprettelse af todimensionel lagdelt Zintl-fase ved dimensionel manipulation af krystalstrukturen
- Mælkevejssatellitterne hjælper med at afsløre forbindelsen mellem mørkt stof-haloer og galakseda…
- Forståelse af magnetismeændringer forårsaget af krystalgitterudvidelse
- Den lyseste kosmiske eksplosion nogensinde:Hvordan vi kan have løst mysteriet, dets forvirrende ved…


