Hvad er pH-værdien af en opløsning med h plus er lig med 7,0 x 10-2?
$$pH =-\log[H^+]$$
hvor [H^+] repræsenterer hydrogenionkoncentrationen i mol pr. liter (mol/L).
Givet [H^+] =7,0 x 10-2 mol/L, kan vi beregne pH:
$$pH =-\log(7,0 \times 10^{-2}) \ca. 1,15$$
Derfor er opløsningens pH cirka 1,15.
Sidste artikelHvad er PH af kirsebær?
Næste artikelHvilke indikatorer bruges til alkalinitetstitrering?
 Varme artikler
Varme artikler
-
 Nye biosensorer opdager hurtigt coronavirus -proteiner og antistofferEn illustration af en ny biosensor, der binder sig til et målrettet molekyle og udsender lys. Oprettelsen af biosensoren blev ledet af UW Medicine Institute for Protein Design. Kredit:Ian Haydon/UW
Nye biosensorer opdager hurtigt coronavirus -proteiner og antistofferEn illustration af en ny biosensor, der binder sig til et målrettet molekyle og udsender lys. Oprettelsen af biosensoren blev ledet af UW Medicine Institute for Protein Design. Kredit:Ian Haydon/UW -
 Forskere finder beviser for metallisk brint ved 425 gigapascalEt udvalg af målinger over det undersøgte trykinterval. en, Fotografier af brintprøven taget på forskellige stadier af komprimering, under samtidig stærk lysbelysning foran og bagpå. Brintprøven er an
Forskere finder beviser for metallisk brint ved 425 gigapascalEt udvalg af målinger over det undersøgte trykinterval. en, Fotografier af brintprøven taget på forskellige stadier af komprimering, under samtidig stærk lysbelysning foran og bagpå. Brintprøven er an -
 Forskere undersøger materialeegenskaber for længerevarende, mere effektive solcellerTidligere postdoktor ved Florida State University, Sarah Wieghold, venstre, og FSU adjunkt i kemi og biokemi Lea Nienhaus. Deres forskning hjælper med at forstå de grundlæggende processer i et materia
Forskere undersøger materialeegenskaber for længerevarende, mere effektive solcellerTidligere postdoktor ved Florida State University, Sarah Wieghold, venstre, og FSU adjunkt i kemi og biokemi Lea Nienhaus. Deres forskning hjælper med at forstå de grundlæggende processer i et materia -
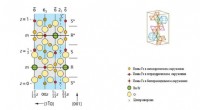 Forskere udvikler materialer til kvanteberegningKrystalstruktur af M-type hexagonal ferrit (en type magnetoplumbit). Kredit:South Ural State University (SUSU) Oprettelse af innovative materialer er et af de vigtigste områder af moderne videnska
Forskere udvikler materialer til kvanteberegningKrystalstruktur af M-type hexagonal ferrit (en type magnetoplumbit). Kredit:South Ural State University (SUSU) Oprettelse af innovative materialer er et af de vigtigste områder af moderne videnska
- Hvordan man laver sjældne jordmagneter
- Når T-celler i vores immunsystem bliver aktive, små trækkræfter på molekylært niveau spiller e…
- Optrævling af historien og videnskaben bag gamle dekorative metaltråde
- Amazon flytter til at oprette sit eget laboratorium til medarbejdernes COVID-19-tests
- Forskere foreslår ti nøglekomponenter til at fremme klimasmart havplanlægning globalt
- 'Byg bedre tilbage' lyder godt i teorien, men ved regeringen virkelig, hvad det betyder praksis?


