Hvad er operationel definition af ph?
En opløsnings pH er et mål for dens surhed eller basicitet og defineres som den negative logaritme (base 10) af hydrogenionkoncentrationen ([H+]). Matematisk kan det udtrykkes som:
pH =-log10[H+]
- Denne definition involverer brug af et pH-meter, et instrument, der måler det elektriske potentiale, der genereres af forskellen i hydrogenionkoncentration mellem en referenceelektrode og en glaselektrode (pH-elektroden).
- Glaselektroden er følsom over for brintioner, og potentialforskellen mellem de to elektroder er direkte proportional med logaritmen af brintionkoncentrationen.
- For at bestemme pH-værdien af en opløsning kalibreres pH-meteret ved hjælp af standardopløsninger med kendt pH, og derefter måles potentialforskellen mellem elektroderne, når pH-elektroden nedsænkes i den relevante opløsning.
- Den målte potentialforskel konverteres til en pH-værdi ved hjælp af kalibreringsdata.
For nøjagtige pH-målinger er det vigtigt at bruge korrekt kalibrerede pH-målere og elektroder, anvende passende teknikker (såsom temperaturkompensation) og følge standardiserede protokoller for at sikre nøjagtighed og pålidelighed.
Sidste artikelHvad er ulemperne ved CO2-renseri?
Næste artikelHvad ER præfikserne for kovalent forbindelse N2O5?
 Varme artikler
Varme artikler
-
 Brug af metal-organiske rammer til at nedbryde plastKredit:Pixabay/CC0 Public Domain Hvad hvis plastikflaskens livscyklus var cirkulær? Hvor en brugt plastikflaske blev returneret til sine originale komponenter, klar til at blive lavet om til en ny
Brug af metal-organiske rammer til at nedbryde plastKredit:Pixabay/CC0 Public Domain Hvad hvis plastikflaskens livscyklus var cirkulær? Hvor en brugt plastikflaske blev returneret til sine originale komponenter, klar til at blive lavet om til en ny -
 Forskere udvikler 3D-printet geléHydrogelmaterialet kommer fra tangpartikler af forskellig størrelse. Kredit:Orlin Velev, NC State University 3D-printbare geler med forbedrede og meget kontrollerede egenskaber kan skabes ved at f
Forskere udvikler 3D-printet geléHydrogelmaterialet kommer fra tangpartikler af forskellig størrelse. Kredit:Orlin Velev, NC State University 3D-printbare geler med forbedrede og meget kontrollerede egenskaber kan skabes ved at f -
 NIST pH standard referencematerialer understøtter en af fremstillingens mest målte egenskaberKredit:National Institute of Standards and Technology NIST har frigivet et pH -referencemateriale i en unikt stabil form til kalibrering af de instrumenter, der bruges af en lang række producenter
NIST pH standard referencematerialer understøtter en af fremstillingens mest målte egenskaberKredit:National Institute of Standards and Technology NIST har frigivet et pH -referencemateriale i en unikt stabil form til kalibrering af de instrumenter, der bruges af en lang række producenter -
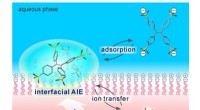 Belysning af vejen til selektiv membranbilleddannelseVandopløselige tetraphenylethen (TPE) derivater, der bærer anioniske grupper, udviser aggregeringsinduceret emission (AIE) adfærd specifikt ved væske-væske-grænseflader. Interfacial AIE-proces reagere
Belysning af vejen til selektiv membranbilleddannelseVandopløselige tetraphenylethen (TPE) derivater, der bærer anioniske grupper, udviser aggregeringsinduceret emission (AIE) adfærd specifikt ved væske-væske-grænseflader. Interfacial AIE-proces reagere
- Resultater fra NASAs Juno opdaterer Jupiter-vandmysteriet
- Fremtidig CO2 og klimaopvarmning potentielt hidtil uset i 420 millioner år
- Forskere bestemmer, hvordan man korrekt fodrer regnbueørred
- Der er fundet beviser på, at Natufian-folk spiser slanger og firben 15, 000 år siden
- Studentbygget satellit har til formål at give indsigt i virkningerne af solstorme
- Hvordan ulidte klasser påvirker snyd for universitetsstuderende


