Hvad er forskellen mellem atomnummer og vægt af kendte grundstoffer som anført i det periodiske system?
1. Atomnummer:
- Et grundstofs atomnummer er repræsenteret ved symbolet "Z" og er lig med antallet af protoner, der findes i et atoms kerne.
- Det er en unik identifikator for hvert grundstof, og ikke to grundstoffer kan have det samme atomnummer.
- Atomnummeret bestemmer grundstoffets placering i det periodiske system. Grundstoffer er arrangeret i stigende rækkefølge efter deres atomnumre.
2. Atomvægt:
- Atomvægten af et grundstof, også kendt som relativ atommasse, er repræsenteret ved symbolet "A" eller "Ar."
- Det er den vægtede gennemsnitlige masse af alle isotoper af et grundstof, under hensyntagen til deres relative overflod.
- Atomvægten betragter bidraget af protoner, neutroner og elektroner i atomet. Imidlertid er massen af elektroner ubetydelig sammenlignet med protoner og neutroner.
- Atomvægten kan være et helt tal eller en decimal afhængig af grundstoffet.
I det periodiske system er atomnummeret normalt angivet over grundstoffets symbol, mens atomvægten er angivet under symbolet.
Her er nogle eksempler for at illustrere forskellen mellem atomnummer og atomvægt:
- Kulstof (C):Atomnummer =6, Atomvægt =12.011
- Ilt (O):Atomnummer =8, Atomvægt =15.999
- Natrium (Na):Atomnummer =11, Atomvægt =22.990
Sammenfattende repræsenterer atomnummeret antallet af protoner og identificerer entydigt hvert element, mens atomvægten repræsenterer den gennemsnitlige masse af alle isotoper af elementet.
 Varme artikler
Varme artikler
-
 Forskere udvikler nyt system til undersøgelse af nye krydsbårne sygdommeKredit:stock.adobe.com Krydsbårne sygdomme er stigende, og især en dukker op i USA og Canada. Human babesiose er en infektion, der kan forårsage en række symptomer og endda døden. Lidt er kendt om
Forskere udvikler nyt system til undersøgelse af nye krydsbårne sygdommeKredit:stock.adobe.com Krydsbårne sygdomme er stigende, og især en dukker op i USA og Canada. Human babesiose er en infektion, der kan forårsage en række symptomer og endda døden. Lidt er kendt om -
 Skinnende røntgenlys på perovskiter for bedre solcellerKredit:CC0 Public Domain Opkaldt efter et mineral opdaget i Uralbjergene i Rusland, perovskites har taget i centrum som en klasse af materialer med egenskaber, der kan anvendes på fremtidige elekt
Skinnende røntgenlys på perovskiter for bedre solcellerKredit:CC0 Public Domain Opkaldt efter et mineral opdaget i Uralbjergene i Rusland, perovskites har taget i centrum som en klasse af materialer med egenskaber, der kan anvendes på fremtidige elekt -
 Forskning i havvands overfladespænding bliver international retningslinjeOverfladespænding er vandets egenskab, der gør det muligt for insekter at skumme vandoverfladen. Forskning udført af John Lienhard og Kishor Nayar for at forstå, hvordan havvandets overfladespænding æ
Forskning i havvands overfladespænding bliver international retningslinjeOverfladespænding er vandets egenskab, der gør det muligt for insekter at skumme vandoverfladen. Forskning udført af John Lienhard og Kishor Nayar for at forstå, hvordan havvandets overfladespænding æ -
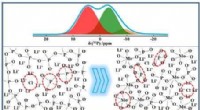 Forskere undersøger strukturen af fosfat-ionisk ledende glas ved hjælp af solid-state NMRStrukturudviklingen af hurtige ionledende glas karakteriseret ved brug af solid-state NMR-teknologier. Kredit:SIOM Glasagtige hurtige ioniske ledere kan bruges som faste elektrolytter, katode ma
Forskere undersøger strukturen af fosfat-ionisk ledende glas ved hjælp af solid-state NMRStrukturudviklingen af hurtige ionledende glas karakteriseret ved brug af solid-state NMR-teknologier. Kredit:SIOM Glasagtige hurtige ioniske ledere kan bruges som faste elektrolytter, katode ma
- Skærende forurening forårsager ikke global opvarmning, undersøgelse finder
- Hvad er den gennemsnitlige procentdel forskel?
- Er kaliumchlorid et upolært molekyle?
- Cambridge Analytica whistleblower opfordrer til online regulering
- Juno-rumfartøjet opdaterer Jupiter-mysteriet fra kvart århundrede
- Google siger, at fejl sendte folks videoer til fremmede


