Hvad er oxidationstallet for kulstof i kulsyre?
I kulsyre er kulstof bundet til to oxygenatomer gennem dobbeltbindinger og til to hydroxylgrupper (OH) gennem enkeltbindinger. Ilts elektronegativitet er højere end kulstof, så oxygenatomerne tiltrækker elektroner væk fra kulstofatomet og giver det en positiv ladning.
Et grundstofs oxidationsnummer repræsenterer antallet af elektroner, som det har fået eller tabt i en forbindelse. I kulsyre har kulstof mistet fire elektroner, to til hvert oxygenatom, hvilket resulterer i et oxidationstal på +4.
Sidste artikelHvad er oxidationstilstanden for calciumhydrid?
Næste artikelHvad er oxidationstallet for C i CO32-?
 Varme artikler
Varme artikler
-
 Brintøkonomi med masseproduktion af højrent brint fra ammoniakAmmoniakbaseret brintekstraktionsanordning. Kredit:Korea Institute of Science and Technology (KIST) Korea Institute of Science and Technology (KIST) har udsendt en meddelelse om teknologien til at
Brintøkonomi med masseproduktion af højrent brint fra ammoniakAmmoniakbaseret brintekstraktionsanordning. Kredit:Korea Institute of Science and Technology (KIST) Korea Institute of Science and Technology (KIST) har udsendt en meddelelse om teknologien til at -
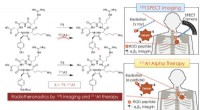 Radioisotoppar til tumordiagnose og terapiKonceptet radiotheranostics ved hjælp af At-211 og I-123 til kræftdiagnose og terapi. Kombination af SPECT-billeddannelse ved hjælp af I-123-mærket RGD-peptid med målrettet alfa-terapi ved hjælp af At
Radioisotoppar til tumordiagnose og terapiKonceptet radiotheranostics ved hjælp af At-211 og I-123 til kræftdiagnose og terapi. Kombination af SPECT-billeddannelse ved hjælp af I-123-mærket RGD-peptid med målrettet alfa-terapi ved hjælp af At -
 Påvisning af blodpletter - med en antimalarial forbindelseAt fortælle hvilken plet på disse papirfiltre (øverste række) er fra blod (C) frem for kaffe (A) eller te (B) er lettere med en ny forbindelse, der reagerer med blod og lyser i mørket (nederste række,
Påvisning af blodpletter - med en antimalarial forbindelseAt fortælle hvilken plet på disse papirfiltre (øverste række) er fra blod (C) frem for kaffe (A) eller te (B) er lettere med en ny forbindelse, der reagerer med blod og lyser i mørket (nederste række, -
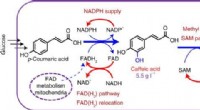 Cofactor engineering driver naturlig produktsynteseGrafisk abstrakt. Kredit:Nature Chemical Biology (2022). DOI:10.1038/s41589-022-01014-6 I det sidste årti har fremskridt inden for syntetisk biologi banet vejen mod bæredygtig syntese af komplekse
Cofactor engineering driver naturlig produktsynteseGrafisk abstrakt. Kredit:Nature Chemical Biology (2022). DOI:10.1038/s41589-022-01014-6 I det sidste årti har fremskridt inden for syntetisk biologi banet vejen mod bæredygtig syntese af komplekse


