Hvilken type binding omkring en central ville resultere i trigonalt plan molekyle -apex?
Ved sp2-hybridisering dannes tre ækvivalente hybridorbitaler ved at blande en s orbitaler og to p-orbitaler. Disse hybridorbitaler danner tre sigma-bindinger med tre andre atomer, hvilket resulterer i en trigonal plan molekylær geometri. Den resterende p-orbital er vinkelret på planet af de tre sp2 hybridorbitaler og kan deltage i pi-binding.
Eksempler på molekyler med trigonal plan molekylær geometri omfatter bortrifluorid (BF3), kuldioxid (CO2) og formaldehyd (H2CO). I disse molekyler er det centrale atom (henholdsvis bor, kulstof og kulstof) sp2 hybridiseret og danner tre sigma-bindinger med de omgivende atomer.
Sidste artikelSammenhæng mellem masse og volumen af en væske?
Næste artikelHvad er de ideelle gaslove?
 Varme artikler
Varme artikler
-
 Bundlemere (nye polymerenheder) kunne transformere industrierEn formel kaldet Thiol-Michael Reaction til konjugering af peptider. Kredit:Kathy F. Atkinson Fra dæk til tøj til shampoo, mange allestedsnærværende produkter fremstilles med polymerer, store kæde
Bundlemere (nye polymerenheder) kunne transformere industrierEn formel kaldet Thiol-Michael Reaction til konjugering af peptider. Kredit:Kathy F. Atkinson Fra dæk til tøj til shampoo, mange allestedsnærværende produkter fremstilles med polymerer, store kæde -
 Nyt værktøj muliggør billeddannelse af neural aktivitet med nær-infrarødt lysRobert Campbell, professor i Institut for Kemi, ledet holdet, der udviklede en ny detektor til at visualisere aktiviteten i neuroner – med applikationer til at hjælpe med at bygge bedre, mere effektiv
Nyt værktøj muliggør billeddannelse af neural aktivitet med nær-infrarødt lysRobert Campbell, professor i Institut for Kemi, ledet holdet, der udviklede en ny detektor til at visualisere aktiviteten i neuroner – med applikationer til at hjælpe med at bygge bedre, mere effektiv -
 4-D printet termit kunne gøre svejsning i rummet og kampzoner lettere, sikrereNeelys har svejst jern (ovenfor) og kobber med den 4D-printede termitpasta. Kredit:Vanderbilt University En nyuddannet maskiningeniør har skabt et materiale til svejsning under ekstreme forhold, s
4-D printet termit kunne gøre svejsning i rummet og kampzoner lettere, sikrereNeelys har svejst jern (ovenfor) og kobber med den 4D-printede termitpasta. Kredit:Vanderbilt University En nyuddannet maskiningeniør har skabt et materiale til svejsning under ekstreme forhold, s -
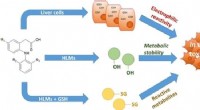 Subtile ændringer i kemisk struktur kan påvirke lægemiddeltoksicitetDerivater af lumiracoxib blev syntetiseret for at forstå forskellige kemiske gruppers bidrag til toksicitet. Forbindelserne blev testet i humane leverceller, og også med og uden tilstedeværelse af glu
Subtile ændringer i kemisk struktur kan påvirke lægemiddeltoksicitetDerivater af lumiracoxib blev syntetiseret for at forstå forskellige kemiske gruppers bidrag til toksicitet. Forbindelserne blev testet i humane leverceller, og også med og uden tilstedeværelse af glu
- Kan du huske, at de sagde, at Miami ville være under vand? En forsmag på fremtiden
- Dreidel-lignende dislokationer fører til bemærkelsesværdige egenskaber
- Sådan fungerer Virtual Reality Gear
- Simulering af dværggalakse afslører forskellige ruter for strontiumberigelse
- Arbejde begynder med ny SLAC -facilitet for revolutionerende acceleratorvidenskab
- Hej DARKNESS:Fysikere går sammen med astronomer om at få bestilt det mest avancerede kamera i verd…


