Hvorfor ændres farven på kobbersulfat, når en jernsøm dyppes i det?
1. Oxidation af jern :Jernmetallet gennemgår en oxidation, hvor dets atomer mister elektroner. Som et resultat omdannes jernatomer til jernholdige (Fe2+) ioner.
2. Reduktion af kobber :I kobbersulfatopløsning får kobberionerne (Cu2+), der er til stede i opløsningen, de elektroner, som jernatomerne taber. Dette resulterer i reduktion af Cu2+ ioner til kobberatomer. Disse kobberatomer danner derefter en belægning af metallisk kobber på overfladen af jernsømmet.
Den overordnede kemiske reaktion kan repræsenteres som:
Fe(s) + CuSO4(aq) → FeSO4(aq) + Cu(s)
Da jernatomer erstatter kobberatomer i kobbersulfat, falmer opløsningens dybblå farve, og en bleggrøn farve af jernsulfatopløsning (FeSO4) er synlig.
Sidste artikelHvilken korrekt metode til at teste lugten af et ukendt kemikalie?
Næste artikelEr hydrogenbromidsyre opløseligt i vand?
 Varme artikler
Varme artikler
-
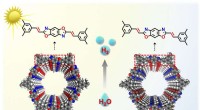 Nye isomere vinylen-bundne kovalente organiske rammer udviklet med distinkte fotokatalytiske egenska…De isomere vinylen-bundne kovalente organiske rammer. Kredit:NIMTE Forskere ledet af prof. Zahng Tao ved Ningbo Institute of Materials Technology and Engineering (NIMTE) fra det kinesiske videnskab
Nye isomere vinylen-bundne kovalente organiske rammer udviklet med distinkte fotokatalytiske egenska…De isomere vinylen-bundne kovalente organiske rammer. Kredit:NIMTE Forskere ledet af prof. Zahng Tao ved Ningbo Institute of Materials Technology and Engineering (NIMTE) fra det kinesiske videnskab -
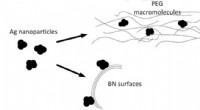 Bornitrid og sølv nanopartikler for at hjælpe med at slippe af med kulilte-emissionerSkemaet med at syntetisere nanohybridkatalysatoren fra lagdelt bornitrid, sølv nanopartikler, og polyethylenglycol. Kredit:Anton S. Konopatsky et al./ Journal of Catalysis , 2018 Russiske kemike
Bornitrid og sølv nanopartikler for at hjælpe med at slippe af med kulilte-emissionerSkemaet med at syntetisere nanohybridkatalysatoren fra lagdelt bornitrid, sølv nanopartikler, og polyethylenglycol. Kredit:Anton S. Konopatsky et al./ Journal of Catalysis , 2018 Russiske kemike -
 Kemikere udnytter kunstig intelligens for at forudsige fremtiden (af kemiske reaktioner)Kredit:CC0 Public Domain Til fremstilling af medicin, kemikere skal finde de rigtige kombinationer af kemikalier for at lave de nødvendige kemiske strukturer. Dette er mere kompliceret end det lyd
Kemikere udnytter kunstig intelligens for at forudsige fremtiden (af kemiske reaktioner)Kredit:CC0 Public Domain Til fremstilling af medicin, kemikere skal finde de rigtige kombinationer af kemikalier for at lave de nødvendige kemiske strukturer. Dette er mere kompliceret end det lyd -
 Spilde bønnerne på kaffens sande identitetKredit:Pixabay/CC0 Public Domain Folk verden over ønsker, at deres kaffe både er tilfredsstillende og til en rimelig pris. For at opfylde disse standarder, ristemaskiner bruger typisk en blanding
Spilde bønnerne på kaffens sande identitetKredit:Pixabay/CC0 Public Domain Folk verden over ønsker, at deres kaffe både er tilfredsstillende og til en rimelig pris. For at opfylde disse standarder, ristemaskiner bruger typisk en blanding
- Brydende bølger driver gamle molekyler op i luften
- Tæmme kulstof nanorør
- Hvordan planter håndterer calcium kan reducere virkningerne af sur regn
- Farvede broderitråde efter behov sparer tid, penge og miljø
- Hvordan Varroa-mider drager fordel af administrerede biavlsmetoder
- Forskere udvikler nyt metamateriale, der kan forbedre MR -kvaliteten og reducere scanningstiden


