Hvordan bestemmes ladningen af atom eller ion ud fra antal protoner, neutroner og elektroner til stede?
1. Protoner:Protoner bærer en positiv elektrisk ladning, så antallet af protoner i et atom eller ion bestemmer dens positive ladning. Hver proton bidrager med en +1 ladning.
2. Elektroner:Elektroner bærer en negativ elektrisk ladning, så antallet af elektroner i et atom eller ion bestemmer dens negative ladning. Hver elektron bidrager med en -1 ladning.
3. Neutroner:Neutroner har ingen elektrisk ladning, så de bidrager ikke til den samlede ladning af et atom eller en ion.
Sådan finder du nettoladningen af et atom eller en ion:
1. Tæl antallet af protoner:Dette giver dig den samlede positive ladning.
2. Tæl antallet af elektroner:Dette giver dig den samlede negative ladning.
3. Træk den samlede negative ladning fra den samlede positive ladning:
- Hvis resultatet er positivt, har atomet eller ionen en netto positiv ladning (kation).
- Hvis resultatet er negativt, har atomet eller ionen en netto negativ ladning (anion).
- Hvis resultatet er nul, har atomet eller ionen ingen nettoladning (neutral).
For eksempel:
1. Neutralt atom:Ilt har 8 protoner (8+) og 8 elektroner (8-). Nettoladningen er 8+ - 8- =0, så oxygen er et neutralt atom.
2. Positiv ion (kation):Natriumion har 11 protoner (11+) og 10 elektroner (10-). Nettoladningen er 11+ - 10- =+1, så natriumion er en kation med en +1 ladning.
3. Negativ ion (anion):Chloridion har 17 protoner (17+) og 18 elektroner (18-). Nettoladningen er 17+ - 18- =-1, så chloridion er en anion med -1 ladning.
Sammenfattende bestemmes ladningen af et atom eller en ion ved at sammenligne antallet af protoner (positiv ladning) med antallet af elektroner (negativ ladning). Nettoladningen kan være positiv, negativ eller nul, hvilket indikerer henholdsvis en kation, anion eller neutralt atom.
Sidste artikelHvilken type bionedbrydelig polymer er der?
Næste artikelHvilken gas findes i køleskabets midterste rum?
 Varme artikler
Varme artikler
-
 Årsag til katodenedbrydning identificeret for nikkelrige materialerMedlemmer af Brookhaven-teamet vises ved NSLS-IIs ISS-strålelinje, hvor en del af undersøgelsen blev udført. På billedet forfra og bagfra ses Eli Stavitski, Xiao-Qing Yang, Xuelong Wang, og Enyuan Hu.
Årsag til katodenedbrydning identificeret for nikkelrige materialerMedlemmer af Brookhaven-teamet vises ved NSLS-IIs ISS-strålelinje, hvor en del af undersøgelsen blev udført. På billedet forfra og bagfra ses Eli Stavitski, Xiao-Qing Yang, Xuelong Wang, og Enyuan Hu. -
 Ny protokol til måling af baggrundsniveauer af stoffer i kriminalitetslaboratorierEn dødelig dosis heroin sammenlignet med en dødelig dosis fentanyl. Dette er kun en illustration - stoffet, der faktisk er vist på dette billede, er et kunstigt sødestof. Kredit:Bruce A. Taylor/NH Sta
Ny protokol til måling af baggrundsniveauer af stoffer i kriminalitetslaboratorierEn dødelig dosis heroin sammenlignet med en dødelig dosis fentanyl. Dette er kun en illustration - stoffet, der faktisk er vist på dette billede, er et kunstigt sødestof. Kredit:Bruce A. Taylor/NH Sta -
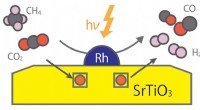 Miljøvenlig katalysator til omdannelse af metan til nyttige gasser ved hjælp af lys i stedet for v…Strontiumtitanat kombineret med rhodiumnanopartikler omdannede metan og kuldioxid til syntesegas under lysbestråling ved meget lavere temperaturer end dem, der kræves i termiske reaktorer. Kredit:Toky
Miljøvenlig katalysator til omdannelse af metan til nyttige gasser ved hjælp af lys i stedet for v…Strontiumtitanat kombineret med rhodiumnanopartikler omdannede metan og kuldioxid til syntesegas under lysbestråling ved meget lavere temperaturer end dem, der kræves i termiske reaktorer. Kredit:Toky -
 Ny kemisk reaktion kan i sidste ende give nye brændstoffer og medicinForskerne fra venstre:Stasik Popov, Alex Bagdasarian, Hosea Nelson og Brian Shao. Kredit:Penny Jennings Når forskere udvikler de kemiske formler til nye produkter som brændstoffer og medicin, de s
Ny kemisk reaktion kan i sidste ende give nye brændstoffer og medicinForskerne fra venstre:Stasik Popov, Alex Bagdasarian, Hosea Nelson og Brian Shao. Kredit:Penny Jennings Når forskere udvikler de kemiske formler til nye produkter som brændstoffer og medicin, de s
- Er ioner til stede i rent flydende HCl?
- Velformet lidelse til alsidige lysteknologier
- Ny og overraskende dualitet fundet i teoretisk partikelfysik
- Hvordan plasmamembranen styrer hvad der kommer ind og kommer ud af en celle
- Billede:En sol om dagen
- Klimaændringer bringer Californias snesæk i fare i fremtidige tørkeperioder


