Hvad er strukturen af SO3 ifølge vesper teori?
```
O=S=O
```
VSEPR-teorien forudsiger, at SO3's molekylære geometri skal være trigonal pyramideformet. Dette skyldes, at svovlatomet har tre elektronpar, der er bundet til atomer, og et ensomt elektronpar. De tre bundne elektronpar er arrangeret i et trigonalt plan, og det enlige elektronpar er placeret i toppen af pyramiden.
Bindingsvinklen i SO3 er 120 grader. Det skyldes, at de tre iltatomer er arrangeret i et trigonalt plan, og det enlige elektronpar på svovlatomet frastøder iltatomerne, hvilket får dem til at bevæge sig tættere sammen.
SO3-molekylet er polært, fordi svovlatomet er mere elektronegativt end oxygenatomerne. Det betyder, at elektronerne i S-O-bindingerne trækkes mod svovlatomet, hvilket skaber en delvis positiv ladning på svovlatomet og en delvis negativ ladning på hvert af iltatomerne.
Dipolmomentet for SO3 er 1,61 D. Dette skyldes, at de tre S-O-bindinger er arrangeret i et trigonalt plan, og det enlige elektronpar på svovlatomet er placeret i toppen af pyramiden. Dette skaber en netto positiv ladning på svovlatomet og en netto negativ ladning på de tre oxygenatomer.
Sidste artikelHvor mange mol opløst stof er der i 50 ml en 12 M HCl-opløsning?
Næste artikelHvad er et stof i alkali?
 Varme artikler
Varme artikler
-
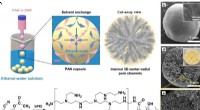 Ny teknologi øger dramatisk genindvindingsgraden af ædle metaller fra affaldFremstillingsprocessen og de fysiske/kemiske strukturer af guldgenvindingsmateriale. Kredit:Korea Institute of Science and Technology (KIST) I Sydkorea, som er afhængig af import for 99,3 % af sine
Ny teknologi øger dramatisk genindvindingsgraden af ædle metaller fra affaldFremstillingsprocessen og de fysiske/kemiske strukturer af guldgenvindingsmateriale. Kredit:Korea Institute of Science and Technology (KIST) I Sydkorea, som er afhængig af import for 99,3 % af sine -
 Forskere udvikler unikt glødende proteinKredit:MIPT Biofysikere fra Moskva Institut for Fysik og Teknologi er gået sammen med kolleger fra Frankrig og Tyskland for at skabe et nyt fluorescerende protein. Udover at gløde, når det bestrål
Forskere udvikler unikt glødende proteinKredit:MIPT Biofysikere fra Moskva Institut for Fysik og Teknologi er gået sammen med kolleger fra Frankrig og Tyskland for at skabe et nyt fluorescerende protein. Udover at gløde, når det bestrål -
 Hurtig og let syntese af antibakteriel aminosyre Schiff-base kobberkomplekserForskere fra Tokyo University of Science brugte en to-trins mikrobølgebestrålingsteknik til at syntetisere aminosyre Schiff base Cu (II) komplekser inden for 10 minutter. De fremstillede baser udviste
Hurtig og let syntese af antibakteriel aminosyre Schiff-base kobberkomplekserForskere fra Tokyo University of Science brugte en to-trins mikrobølgebestrålingsteknik til at syntetisere aminosyre Schiff base Cu (II) komplekser inden for 10 minutter. De fremstillede baser udviste -
 Forskere udvikler en ny metode til forbedring af effektiviteten af luftrensereLuftrenser. Kredit:Sergei Preis, TalTech Ren luft er noget, vi løbende er stolte af i vores lille Estland, og det er blevet kaldt, dels i sjov, en af de vigtigste eksport. Desværre, miljøet, her
Forskere udvikler en ny metode til forbedring af effektiviteten af luftrensereLuftrenser. Kredit:Sergei Preis, TalTech Ren luft er noget, vi løbende er stolte af i vores lille Estland, og det er blevet kaldt, dels i sjov, en af de vigtigste eksport. Desværre, miljøet, her
- Hvad bidrog John Dalton til forståelsen af atomet?
- Forskere rapporterer mere præcis måling af neutroner
- At fange lys:Hvordan kobolt kan hjælpe med at udnytte synligt lys til at drive brintproduktion fra …
- Måder at bestemme Density
- Indonesiens kvinder står over for daglig svømning efter rent vand
- Vil du gøre noget ved den globale opvarmning? Tal om det med din familie og venner


