Hvorfor findes alkaliske metaller ikke frie i naturen?
Derudover er alkalimetaller også relativt bløde og har et lavt smeltepunkt. Det betyder, at de let deformeres og kan smelte ved relativt lave temperaturer. Dette gør dem uegnede til brug i mange applikationer, hvor der kræves et stærkt, hårdt materiale.
Endelig er alkaliske metaller også meget brandfarlige. Det betyder, at de nemt kan antændes og brænde ved høj temperatur. Dette gør dem til en sikkerhedsrisiko og begrænser deres brug i mange applikationer.
Sidste artikelHvorfor findes metallisk natrium ikke i naturen?
Næste artikelHvorfor flyder nogle væsker langsommere end andre?
 Varme artikler
Varme artikler
-
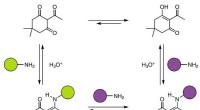 Kemikere fremstiller termohærdende polymer ved hjælp af amin og triketon, der kan genbrugesVendbar, dynamiske kovalente diketoenaminbindinger. Diketoenaminbindinger dannes spontant fra triketoner og både aromatiske og alifatiske aminer. Under stærkt sure forhold i vand, diketoenaminbindinge
Kemikere fremstiller termohærdende polymer ved hjælp af amin og triketon, der kan genbrugesVendbar, dynamiske kovalente diketoenaminbindinger. Diketoenaminbindinger dannes spontant fra triketoner og både aromatiske og alifatiske aminer. Under stærkt sure forhold i vand, diketoenaminbindinge -
 Forskere finder potentielt manglende led i kemi, der førte til liv på JordenKredit:CC0 Public Domain Kemikere ved The Scripps Research Institute (TSRI) har fundet en forbindelse, der kan have været en afgørende faktor i livets oprindelse på Jorden. Forskere fra livets op
Forskere finder potentielt manglende led i kemi, der førte til liv på JordenKredit:CC0 Public Domain Kemikere ved The Scripps Research Institute (TSRI) har fundet en forbindelse, der kan have været en afgørende faktor i livets oprindelse på Jorden. Forskere fra livets op -
 Forskere udvikler lagdelt koboltoxid med en rekordhøj termoelektrisk værdiBarium-koboltoxidfilmen (øverst til højre, ca. 1 cm2) udsættes for åben ild for at generere spænding. Kredit:Hiromichi Ohta Spildvarme er en meget lovende kilde til vedvarende energi; imidlertid,
Forskere udvikler lagdelt koboltoxid med en rekordhøj termoelektrisk værdiBarium-koboltoxidfilmen (øverst til højre, ca. 1 cm2) udsættes for åben ild for at generere spænding. Kredit:Hiromichi Ohta Spildvarme er en meget lovende kilde til vedvarende energi; imidlertid, -
 En mulig afslutning på evige kemikalierKredit:Marla Bereni/UCR Syntetiske kemikalier kendt som per- og polyfluoralkyler, eller PFAS, indeholder bindinger mellem kulstof- og fluoratomer, der anses for at være de stærkeste i organisk kem
En mulig afslutning på evige kemikalierKredit:Marla Bereni/UCR Syntetiske kemikalier kendt som per- og polyfluoralkyler, eller PFAS, indeholder bindinger mellem kulstof- og fluoratomer, der anses for at være de stærkeste i organisk kem
- Ubetalt fri fra arbejde steg 50 % under pandemi
- Lille skala, store forbedringer
- FIFA giver VAR grønt lys ved VM
- I byer, farlig varmeeksponering er tredoblet siden 1980'erne, med de fattigste mest udsatte
- Risikabel forretning:Nye data viser, hvordan søkoer bruger forsendelseskanaler
- UAE nægter at udvikle den populære Mideast -app som spionværktøj


