Hvor mange uparrede elektroner er der i et koboltatoms grundtilstand?
[Ar] 3d^7 4s^2
I denne konfiguration er 3d orbitaler delvist udfyldt. 3d orbitaler består af fem degenererede orbitaler, og de syv elektroner i kobolts 3d orbitaler fordeler sig blandt disse orbitaler på en måde, der minimerer elektron-elektron frastødningen.
Ifølge Hunds regel har elektroner i samme orbital en tendens til at have samme spin, men med den maksimalt mulige spin-multiplicitet. Med andre ord vil elektroner optage degenererede orbitaler enkeltvis før parring.
I kobolts tilfælde optager de syv 3d-elektroner de fem 3d-orbitaler, hvor fire af elektronerne har deres spins justeret i én retning (spin-up), og de resterende tre elektroner har deres spins justeret i den modsatte retning (spin-down).
Derfor har et koboltatom i sin grundtilstand tre uparrede elektroner .
Sidste artikelHvordan afbalancerer du kemikalierne i Bor og H2O?
Næste artikelHvad og skaber en ionbinding?
 Varme artikler
Varme artikler
-
 Forskere udvikler 3D-printet geléHydrogelmaterialet kommer fra tangpartikler af forskellig størrelse. Kredit:Orlin Velev, NC State University 3D-printbare geler med forbedrede og meget kontrollerede egenskaber kan skabes ved at f
Forskere udvikler 3D-printet geléHydrogelmaterialet kommer fra tangpartikler af forskellig størrelse. Kredit:Orlin Velev, NC State University 3D-printbare geler med forbedrede og meget kontrollerede egenskaber kan skabes ved at f -
 Forskere bruger mikrobølger til at måle tegn på dehydreringBillede, der viser mikrobølgesensorteknologisystem, der måler dråbe blod. Kredit:Queen Mary, University of London London og National Physical Laboratory (NPL) har med succes brugt mikrobølger til
Forskere bruger mikrobølger til at måle tegn på dehydreringBillede, der viser mikrobølgesensorteknologisystem, der måler dråbe blod. Kredit:Queen Mary, University of London London og National Physical Laboratory (NPL) har med succes brugt mikrobølger til -
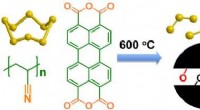 Svovl giver et lovende næste generations batterialternativEn skematisk illustration af dannelsen af kemisk bindingsstabiliseret kulstof-svovlkomposit. Kredit:C. Luo Med den stigende efterspørgsel efter økonomisk overkommelig og bæredygtig energi, den l
Svovl giver et lovende næste generations batterialternativEn skematisk illustration af dannelsen af kemisk bindingsstabiliseret kulstof-svovlkomposit. Kredit:C. Luo Med den stigende efterspørgsel efter økonomisk overkommelig og bæredygtig energi, den l -
 Bindingsdissociationsenergier for overgangsmetalsilicider er nøjagtigt bestemtKredit:CC0 Public Domain Overgangsmetal silicider, en særskilt klasse af halvledende materialer, der indeholder silicium, demonstrere overlegen oxidationsmodstand, høj temperaturstabilitet og lave
Bindingsdissociationsenergier for overgangsmetalsilicider er nøjagtigt bestemtKredit:CC0 Public Domain Overgangsmetal silicider, en særskilt klasse af halvledende materialer, der indeholder silicium, demonstrere overlegen oxidationsmodstand, høj temperaturstabilitet og lave
- Historien om, hvordan swahili blev Afrikas mest talte sprog
- Ny forskning viser, at grafen kan fungere som overfladeaktivt stof
- Forskere i Asien genoptog arbejdet langt hurtigere end vestlige kolleger, viser international COVID …
- Forskere ser smeltede salte skære små kroge og tunneler ind i metallegeringer i 3D
- Forskel på jordskælv for- og efterskælv
- Video-artikel viser, hvordan man renser magnetiske bakterier


