Hvordan forudsiger man den korrekte formel for kombinationsreaktion mellem et ikke-metal og gruppe A-metal?
1. Identificer ikke-metallet og det involverede gruppe A-metal.
2. Bestem ladningerne af ikke-metal- og gruppe A-metalionerne.
3. Brug metoden på kryds og tværs til at bestemme den empiriske formel for forbindelsen.
Overvej for eksempel reaktionen mellem natrium (et gruppe A-metal) og klor (et ikke-metal).
1. Natrium har en ladning på +1, mens klor har en ladning på -1.
2. For at balancere ladningerne har vi brug for et natriumatom for hvert et kloratom.
3. Den empiriske formel for den dannede forbindelse er derfor NaCl.
Den samme tilgang kan bruges til at forudsige den korrekte formel for enhver kombinationsreaktion mellem et ikke-metal og et gruppe A-metal.
Sidste artikelEr masse og volumen en kemisk egenskab?
Næste artikelHvad er betydningen af kemi i informationsteknologi?
 Varme artikler
Varme artikler
-
 Forskere skaber kunstig perlemor ved hjælp af bakterierDenne abalone skal er en naturlig form for nacre-også kendt som perlemor-et usædvanligt hårdt materiale, der findes i skaller og perler. Rochester biologer har udviklet en innovativ metode til at skab
Forskere skaber kunstig perlemor ved hjælp af bakterierDenne abalone skal er en naturlig form for nacre-også kendt som perlemor-et usædvanligt hårdt materiale, der findes i skaller og perler. Rochester biologer har udviklet en innovativ metode til at skab -
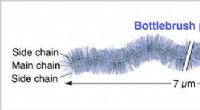 Verdens længste flaskebørstepolymer nogensinde syntetiseretFlaskebørstepolymer er en polymer bestående af en enkelt hovedkæde og adskillige sidekæder podet fra hovedkæden. Kredit:National Institute for Materials Science NIMS og RIKEN er lykkedes med at sy
Verdens længste flaskebørstepolymer nogensinde syntetiseretFlaskebørstepolymer er en polymer bestående af en enkelt hovedkæde og adskillige sidekæder podet fra hovedkæden. Kredit:National Institute for Materials Science NIMS og RIKEN er lykkedes med at sy -
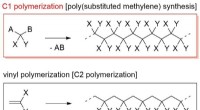 Udvikling af nye smarte bløde materialer:Syntese af en pH-reagerende dendroniseret poly(substituere…Vinylpolymerisation og C1-polymerisation. Kredit:Ehime Unisity C1-polymerisation er en nyttig teknik til fremstilling af polymerer med en carbon-carbon-hovedkæde. Denne teknik konstruerer en polym
Udvikling af nye smarte bløde materialer:Syntese af en pH-reagerende dendroniseret poly(substituere…Vinylpolymerisation og C1-polymerisation. Kredit:Ehime Unisity C1-polymerisation er en nyttig teknik til fremstilling af polymerer med en carbon-carbon-hovedkæde. Denne teknik konstruerer en polym -
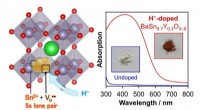 Vellykket syntese af perovskit synligt lysabsorberende halvledermaterialeEt billigere perovskit-baseret halvledermateriale, der er fri for giftigt bly og kan absorbere en bred vifte af synligt lys med potentielle fotofunktionelle applikationer. Kredit:Materialekemi Hal
Vellykket syntese af perovskit synligt lysabsorberende halvledermaterialeEt billigere perovskit-baseret halvledermateriale, der er fri for giftigt bly og kan absorbere en bred vifte af synligt lys med potentielle fotofunktionelle applikationer. Kredit:Materialekemi Hal
- Vampyralgedræberens genetiske mangfoldighed udgør en trussel mod biobrændstoffer
- NASA konstaterer, at den tropiske storm Maliksi svækkes, udvides
- Hvad er den gennemsnitlige årlige nedbør i Sahara-ørkenen?
- Nøgleegenskaber ved grafen opretholdes over brede intervaller af tæthed og energi
- Saturns måne er et forsøgssted for at få en bedre forståelse af metanmolekylet
- Algoritmer opsøger vælgersvindel


