Hvad er opløseligheden af magnesiumoxid?
Opløseligheden af MgO kan beregnes ved hjælp af Ksp-udtrykket:
Ksp =[Mg 2+ ][OH - ]^2
Ved ligevægt er koncentrationen af Mg 2+ og OH - ioner vil være ens, så vi kan erstatte [Mg 2+ ] =[OH - ] =x.
Ksp =x^3
x =[Mg 2+ ] =[OH - ] =(Ksp) 1/3
Ved at erstatte værdien af Ksp får vi:
x =(5,61 x 10 -12 ) 1/3 =1,83 x 10 -4 M
Derfor er opløseligheden af magnesiumoxid i vand ved 25 °C ca. 1,83 x 10 -4 M.
Sidste artikelSvaret, når svovlsyre nedbrydes til fom svovltrioxidgas plus vand?
Næste artikelHvad er Lewis-strukturen for SiCl2Br2?
 Varme artikler
Varme artikler
-
 Design af selektive membraner til batterier ved hjælp af en værktøjskasse til opdagelse af lægem…Illustration af litiumioner i bur i en ny polymermembran til lithiumbatterier. Forskere ved Berkeley Labs Molecular Foundry brugte en værktøjskasse til opdagelse af lægemidler til at designe de selekt
Design af selektive membraner til batterier ved hjælp af en værktøjskasse til opdagelse af lægem…Illustration af litiumioner i bur i en ny polymermembran til lithiumbatterier. Forskere ved Berkeley Labs Molecular Foundry brugte en værktøjskasse til opdagelse af lægemidler til at designe de selekt -
 Små molekylære bevægelser kan føre til mere effektive biobrændselscellerKredit:Leiden Universitet Leiden-forskere har fundet små bevægelser i laccase-enzymet. Denne opdagelse kan føre til udviklingen af meget mere effektive biobrændselsceller. Udgivelse i Biofysisk
Små molekylære bevægelser kan føre til mere effektive biobrændselscellerKredit:Leiden Universitet Leiden-forskere har fundet små bevægelser i laccase-enzymet. Denne opdagelse kan føre til udviklingen af meget mere effektive biobrændselsceller. Udgivelse i Biofysisk -
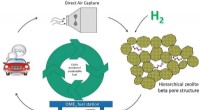 Vejen til at opnå netto-flydende brændstofEn grafisk fremstilling af, hvordan kuldioxid kan omdannes til et dieselbrændstof. Kredit:Monash University Forskere fra Monash University og Hokkaido University har udviklet en metode, der omdann
Vejen til at opnå netto-flydende brændstofEn grafisk fremstilling af, hvordan kuldioxid kan omdannes til et dieselbrændstof. Kredit:Monash University Forskere fra Monash University og Hokkaido University har udviklet en metode, der omdann -
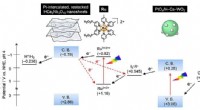 Ny fotokatalysator øger vandspaltningseffektiviteten til ren brintproduktionOxygenudviklingskatalysatoren reducerer effektivt koncentrationen af I3 - ioner og ændringer i hydrogenudviklingskatalysatoren forhindrer elektrontilbageførsel (stiplede røde linjer) og prioriterer
Ny fotokatalysator øger vandspaltningseffektiviteten til ren brintproduktionOxygenudviklingskatalysatoren reducerer effektivt koncentrationen af I3 - ioner og ændringer i hydrogenudviklingskatalysatoren forhindrer elektrontilbageførsel (stiplede røde linjer) og prioriterer
- Er tyngdepunktet en meterstok altid placeret ved 50-cm-mærket?
- Spørg os om følgende er sande om centripetalkraft?
- Forskere finder det manglende fotoniske link for at muliggøre et kvanteinternet i silicium
- Blyhvide pigmenter på Andes drikkekar giver ny historisk kontekst
- Forvrængende virkninger af kortdistancefotografier på nasal udseende:Selfie -effekten
- Californien er unormalt tør efter vinter med lav nedbør


