Hvilken betydning havde det periodiske system for kemikere?
1. Organisation af elementer:
Det periodiske system organiserer alle elementerne på en logisk og struktureret måde, hvilket gør det lettere at studere og sammenligne deres egenskaber. Den kategoriserer elementer i grupper (lodrette kolonner) og perioder (vandrette rækker) baseret på fælles kemiske egenskaber. Denne systematiske organisation forenkler opgaven med at identificere tendenser og mønstre i elementernes adfærd.
2. Forståelse af egenskaber og reaktivitet:
Det periodiske system giver indsigt i grundstoffernes egenskaber og reaktivitet. Ved at undersøge et elements position i tabellen kan kemikere hurtigt vurdere dets valenselektronkonfiguration, som bestemmer dets kemiske adfærd. For eksempel har grundstoffer i den samme gruppe en tendens til at have lignende valenselektronkonfigurationer og viser således lignende kemiske egenskaber.
3. Gruppeligheder og periodicitet:
Det periodiske system afslører periodiske tendenser i grundstoffernes egenskaber. Grundstoffer i en gruppe (lodret søjle) deler lignende kemiske egenskaber på grund af at have det samme antal valenselektroner. Når man bevæger sig ned ad en gruppe, bliver grundstofferne mere metalliske, større i atomstørrelse og udviser lavere ioniseringsenergier. Omvendt viser flytning på tværs af en periode (vandret række) en gradvis ændring i egenskaber, efterhånden som atomnummeret stiger.
4. Forudsigelse og opdagelse af nye elementer:
Det periodiske system gør det muligt for kemikere at forudsige eksistensen og egenskaberne af nye grundstoffer, før de opdages. Huller i tabellen indikerer muligheden for uopdagede elementer, der vejleder forskere i deres søgning. Når nye grundstoffer syntetiseres eller findes i naturen, kan deres positioner i det periodiske system forudsiges nøjagtigt baseret på deres atomnumre og kemiske egenskaber.
5. Forståelse af kemisk binding og reaktioner:
Det periodiske system hjælper kemikere med at forstå og forudsige kemiske bindinger og reaktioner. Valenselektronkonfigurationer spiller en afgørende rolle i bestemmelsen af de typer bindinger, som et grundstof kan danne, og dets reaktivitet. Ved at sammenligne elektronkonfigurationerne af forskellige grundstoffer kan kemikere forudse de dannede bindinger og forbindelsernes stabilitet.
6. Undervisning og læring i kemi:
Det periodiske system er et stærkt værktøj til at undervise og lære kemi. Det giver en visuel repræsentation af forholdet mellem elementer og deres egenskaber, hvilket gør komplekse koncepter mere tilgængelige og lettere at forstå. Organiseringen af det periodiske system giver eleverne mulighed for at lære om grundstoffernes egenskaber og tendenser på en systematisk måde.
Sammenfattende er det periodiske system en uvurderlig ressource for kemikere. Det organiserer elementer, afslører tendenser og mønstre i deres egenskaber, hjælper med at forstå kemiske bindinger og reaktioner og letter opdagelsen af nye grundstoffer. Dens betydning strækker sig til forskellige kemiområder, herunder uorganisk kemi, organisk kemi, biokemi og mange flere.
Sidste artikelHvor mange blandinger er der?
Næste artikelHvad er homogen væske?
 Varme artikler
Varme artikler
-
 Sådan bukker du fladt glas perfekt rundt om hjørnerEt dobbeltglas hjørneelement produceret med den nye glasbukkeproces. Kredit:Fraunhofer IWM Forskere fra Fraunhofer Institute for Mechanics of Materials IWM har udviklet en ny proces, der kan bøje
Sådan bukker du fladt glas perfekt rundt om hjørnerEt dobbeltglas hjørneelement produceret med den nye glasbukkeproces. Kredit:Fraunhofer IWM Forskere fra Fraunhofer Institute for Mechanics of Materials IWM har udviklet en ny proces, der kan bøje -
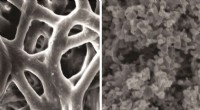 Mikroskopisk membran kan bekæmpe tandkødssygdommeBilleder af holdets membran (til venstre) og zink-nanopartiklerne (til højre) indlejret i den. Kredit:Advanced Functional Materials / Wiley-VCH Paradentose – en fremskreden form for tandkødssygdom
Mikroskopisk membran kan bekæmpe tandkødssygdommeBilleder af holdets membran (til venstre) og zink-nanopartiklerne (til højre) indlejret i den. Kredit:Advanced Functional Materials / Wiley-VCH Paradentose – en fremskreden form for tandkødssygdom -
 Sensorer registrerer sygdomsmarkører i åndedrættetForskerne lavede sensorer af porøse tynde film af organisk ledende plast med målet om bærbar, engangsudstyr til medicinsk og miljømæssig overvågning. Kredit:L. Brian Stauffer En lille, tynd firkan
Sensorer registrerer sygdomsmarkører i åndedrættetForskerne lavede sensorer af porøse tynde film af organisk ledende plast med målet om bærbar, engangsudstyr til medicinsk og miljømæssig overvågning. Kredit:L. Brian Stauffer En lille, tynd firkan -
 Lignin – et supergrønt brændstof til brændselscellerKredit:Linköping Universitet Forskere fra Laboratory of Organic Electronics ved Linköpings Universitet har udviklet en brændselscelle, der bruger lignin, et billigt biprodukt fra papirfremstilling
Lignin – et supergrønt brændstof til brændselscellerKredit:Linköping Universitet Forskere fra Laboratory of Organic Electronics ved Linköpings Universitet har udviklet en brændselscelle, der bruger lignin, et billigt biprodukt fra papirfremstilling
- Tyrkisk højesteret vil gennemgå Wikipedias appel mod forbud
- Rejser du til Mars i dine drømme?
- Det vedvarende problem med 1, 4-dioxan i vand
- I løbet af hvad overføres elektroner og frigives energi?
- NASA nordlige kvadrantstyrke i Tropical Cyclone Lili
- Meget forbedrede klimaforudsigelser fra statistisk mekanik


