Hvilke former for intermolekylære kræfter er til stede i en blanding af calciumbromid og vand?
1. Ion-dipolkræfter :Disse kræfter er til stede mellem de positivt ladede calciumioner (Ca2+) og de polære vandmolekyler. Vandmolekylerne har en lille negativ ladning på grund af iltens elektronegativitet, og de tiltrækkes af calciumionernes positive ladning.
2. Dipol-dipolkræfter :Disse kræfter er til stede mellem de polære vandmolekyler. Vandmolekylerne har et permanent dipolmoment på grund af forskellen i elektronegativitet mellem ilt og brint. Den positive ende af et vandmolekyle tiltrækkes af den negative ende af et andet vandmolekyle.
3. Brintbinding :Dette er en speciel type dipol-dipolkraft, der opstår, når et hydrogenatom er kovalent bundet til et stærkt elektronegativt atom såsom oxygen, nitrogen eller fluor. I tilfælde af calciumbromid og vand sker der hydrogenbinding mellem vandmolekylerne. Hydrogenatomet i vandmolekylet er kovalent bundet til oxygenatomet, og det har en let positiv ladning. Denne positive ladning tiltrækkes af den negative ladning af oxygenatomet i et andet vandmolekyle og danner en hydrogenbinding.
Kombinationen af disse intermolekylære kræfter resulterer i dannelsen af en stabil blanding af calciumbromid og vand. Ionkræfterne mellem calciumionerne og vandmolekylerne er stærke, og dipol-dipolkræfterne og hydrogenbindingen mellem vandmolekylerne er med til at stabilisere blandingen yderligere.
Sidste artikelKan jernoxid bruges som medicin?
Næste artikelEr methanol et mættet eller umættet kulbrinte?
 Varme artikler
Varme artikler
-
 Klarere og bedre fokuserede SEM-billederKredit:Pohang University of Science &Technology (POSTECH) Med begyndelsen af den 4. industrielle revolution, kunstig intelligens er for nylig blevet brugt i smartphone -kameraer, leverer funktio
Klarere og bedre fokuserede SEM-billederKredit:Pohang University of Science &Technology (POSTECH) Med begyndelsen af den 4. industrielle revolution, kunstig intelligens er for nylig blevet brugt i smartphone -kameraer, leverer funktio -
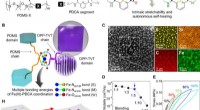 Strækbar, selvhelbredende og halvledende polymerfilm til elektronisk hud (e-skin)Design og karakterisering af belastningsfølsomme, strækbar, og selvhelbredende halvledende film. (A) Kemisk struktur af DPP halvledende polymer, PDMS, og PDCA-del introduceret i begge polymerskeletter
Strækbar, selvhelbredende og halvledende polymerfilm til elektronisk hud (e-skin)Design og karakterisering af belastningsfølsomme, strækbar, og selvhelbredende halvledende film. (A) Kemisk struktur af DPP halvledende polymer, PDMS, og PDCA-del introduceret i begge polymerskeletter -
 Forståelse af vands mærkelige adfærdEn clathrate is, med oxygener repræsenteret som kugler, og hydrogenbindinger som linier. Arbejdet har vist, hvordan komplekse krystallinske strukturer opstår som følge af vands interaktioner. Kredit:U
Forståelse af vands mærkelige adfærdEn clathrate is, med oxygener repræsenteret som kugler, og hydrogenbindinger som linier. Arbejdet har vist, hvordan komplekse krystallinske strukturer opstår som følge af vands interaktioner. Kredit:U -
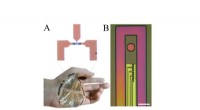 To trin tættere på fleksibel, magtfulde, hurtige bioelektroniske enhederForenelig enhancement-mode, intern ion-gated organisk elektrokemisk transistor (e-IGT) A) Mikrograf, der viser ovenfra en e-IGT (top). Skala bar, 5 μm. Ultra-fleksibel, ultratyndt e-IGT-array i overen
To trin tættere på fleksibel, magtfulde, hurtige bioelektroniske enhederForenelig enhancement-mode, intern ion-gated organisk elektrokemisk transistor (e-IGT) A) Mikrograf, der viser ovenfra en e-IGT (top). Skala bar, 5 μm. Ultra-fleksibel, ultratyndt e-IGT-array i overen
- Kryptovaluta blæser i vinden, da min åbner i Estland
- Routergæstnetværk mangler tilstrækkelig sikkerhed, ifølge forskere
- Interaktioner mellem simple molekylære mekanismer giver anledning til kompleks infektionsdynamik
- Livscyklus af Sloths
- En ny bioproces til at omdanne plantematerialer til værdifulde kemikalier
- Kan Kina holde sine klimaløfter?


