Hvorfor synker nogle væsker under vand?
Vand har en massefylde på cirka 1 gram pr. kubikcentimeter (g/cm³). Væsker, der er tættere end vand, vil bundfælde sig i bunden, når de kombineres på grund af tyngdekraften. For eksempel er kviksølv et flydende metal med en densitet på cirka 13,6 g/cm³, hvilket gør det til en af de tætteste væsker ved stuetemperatur. Når det placeres i vand, vil kviksølv danne tydelige kugler og synke, fordi dets tæthed er meget højere.
Her er et par eksempler på væsker, der er tættere end vand, der vil synke:
1. Kviksølv (Hg) :Massefylde =13,6 g/cm³
2. Gallium (Ga) :Massefylde =5,91 g/cm³ (i flydende tilstand)
3. Natrium (Na) :Massefylde =0,97 g/cm³ (i flydende tilstand)
4. Kalium (K) :Massefylde =0,86 g/cm³ (i flydende tilstand)
Det er vigtigt at bemærke, at nogle væsker, såsom olie eller alkohol, er mindre tætte end vand og vil flyde oven på det i stedet for at synke. Den relative tæthed af væsker bestemmer deres adfærd, når de blandes sammen.
Sidste artikelKunne du finde en videnskabelig sætning med ordet opdrift?
Næste artikelHvad er isolerende pakning?
 Varme artikler
Varme artikler
-
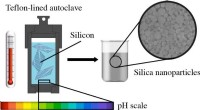 En miljøvenlig måde at omdanne silicium til nanopartiklerKredit:Skolkovo Institute of Science and Technology Skoltech -forskere og deres kolleger fra Lomonosov Moscow State University (MSU) har udviklet en ny metode til genbrug af silicium. Deres forskn
En miljøvenlig måde at omdanne silicium til nanopartiklerKredit:Skolkovo Institute of Science and Technology Skoltech -forskere og deres kolleger fra Lomonosov Moscow State University (MSU) har udviklet en ny metode til genbrug af silicium. Deres forskn -
 Nanopartikler har brug for lidt plads til at overføre energiForskere viser, hvordan energi bevæger sig (grøn) eller ikke (rød) langs nanopartikelkæder. Kredit:Journal of Materials Chemistry C. Royal Society of Chemistry Hurtig overførsel af energi fra et s
Nanopartikler har brug for lidt plads til at overføre energiForskere viser, hvordan energi bevæger sig (grøn) eller ikke (rød) langs nanopartikelkæder. Kredit:Journal of Materials Chemistry C. Royal Society of Chemistry Hurtig overførsel af energi fra et s -
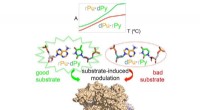 Forskere identificerer kilden til asymmetri i RNA-DNA-hybriderAsymmetrien af DNA-RNA-hybrider kan bruges til at forbedre effektiviteten af genredigeringsteknologier som CRISPR-Cas9. Kredit:Institut for Forskning i Biomedicin-IRB En undersøgelse ledet af
Forskere identificerer kilden til asymmetri i RNA-DNA-hybriderAsymmetrien af DNA-RNA-hybrider kan bruges til at forbedre effektiviteten af genredigeringsteknologier som CRISPR-Cas9. Kredit:Institut for Forskning i Biomedicin-IRB En undersøgelse ledet af -
 Bladvenestruktur kan være nøglen til at forlænge batteriets levetidNærbillede af et blad, der viser sine årer. Kredit:Christoph Rupprecht/Flickr Den naturlige struktur, der findes i blade, kan forbedre alt fra genopladelige batterier til højtydende gassensorer, i
Bladvenestruktur kan være nøglen til at forlænge batteriets levetidNærbillede af et blad, der viser sine årer. Kredit:Christoph Rupprecht/Flickr Den naturlige struktur, der findes i blade, kan forbedre alt fra genopladelige batterier til højtydende gassensorer, i
- Lufthansa tilbyder klimavenligt brændstof, men til en pris
- Undersøgelse viser, hvordan fugleinfluenza kan udryddes ved at redigere generne fra høns
- Baby boomere eller millennials? Fire generationer er i dagens arbejdsstyrke
- Bekæmpelse af antibiotikaresistens:Fag-lignende antibakterielle kerne-skal nanopartikler kunne hjæ…
- Hvad vejrmænd ved om klimaændringer
- Amerikanske gratis nyhedswebsteder BuzzFeed, HuffPost mærker afskedigelsen knibe


