Hvad er den samlede prøvestørrelse (i gram) for en ethanol (CH3CH2OH), som indeholder 3,36 g oxygen?
Ethanols molekylære formel er CH3CH2OH, hvilket indikerer, at hvert molekyle består af 2 carbonatomer (C), 6 hydrogenatomer (H) og 1 oxygenatom (O).
Lad os beregne molmassen af ethanol:
Molær masse af C =12,01 g/mol
Molær masse af H =1,01 g/mol
Molær masse af O =16,00 g/mol
Molær masse af ethanol (CH3CH2OH) =(2 x 12,01 g/mol) + (6 x 1,01 g/mol) + (1 x 16,00 g/mol)
=24,02 g/mol + 6,06 g/mol + 16,00 g/mol
=46,08 g/mol
Lad os nu bestemme masseprocenten af oxygen i ethanol:
Masseprocent af oxygen =(iltmasse i ethanol / molær masse af ethanol) x 100 %
=(16,00 g/mol / 46,08 g/mol) x 100 %
=34,72 %
Da vi ved, at prøven indeholder 3,36 g ilt, kan vi beregne den samlede prøvestørrelse (i gram) ved hjælp af masseprocenten af ilt:
Samlet prøvestørrelse =(iltmasse / masseprocent ilt) x 100 %
=(3,36 g / 34,72 %) x 100 %
=9,68 g
Derfor er den samlede prøvestørrelse for ethanolprøven indeholdende 3,36 g oxygen 9,68 gram.
Sidste artikelNår du hælder kalium pr. magnat i vand, skifter det til hvilken farve?
Næste artikelHvor er kemisk forvitring mest aktiv?
 Varme artikler
Varme artikler
-
 Ny vandspaltningskatalysator kunne gøre det lettere at generere solbrændstofBinghamton University lektor i fysik Louis Piper. Kredit:Binghamton University, State University of New York Vandspaltning, processen med at høste solenergi for at generere energitætte brændstoffe
Ny vandspaltningskatalysator kunne gøre det lettere at generere solbrændstofBinghamton University lektor i fysik Louis Piper. Kredit:Binghamton University, State University of New York Vandspaltning, processen med at høste solenergi for at generere energitætte brændstoffe -
 Surroundlyd fra letvægts rulle-til-rulle trykt højttalerpapirTrykte højttalere skaber overraskende jungle-illusion. Trykt elektronik indlejret i en papirbane muliggør 360° surroundsound. Varvara Bachul fra Institute of Print and Media Technology ved Chemnitz Un
Surroundlyd fra letvægts rulle-til-rulle trykt højttalerpapirTrykte højttalere skaber overraskende jungle-illusion. Trykt elektronik indlejret i en papirbane muliggør 360° surroundsound. Varvara Bachul fra Institute of Print and Media Technology ved Chemnitz Un -
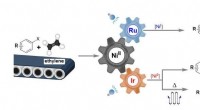 Katalytisk omdannelse af ethylenIllustration, der viser de nikkelkatalyserede reaktioner mellem kommercielt tilgængeligt arylhalogenid og ethylen. Oxidationstilstanden af nikkelkatalysatoren ændres til +1 eller 0, når den modulere
Katalytisk omdannelse af ethylenIllustration, der viser de nikkelkatalyserede reaktioner mellem kommercielt tilgængeligt arylhalogenid og ethylen. Oxidationstilstanden af nikkelkatalysatoren ændres til +1 eller 0, når den modulere -
 Teknik kan gøre det lettere at bruge mRNA til at behandle sygdom eller levere vacciner”Hvis vi vil være i stand til at levere mRNA, så har vi brug for en mekanisme til at være mere effektiv til det, fordi alt, hvad der har været brugt indtil nu, giver dig en meget lille brøkdel af, hva
Teknik kan gøre det lettere at bruge mRNA til at behandle sygdom eller levere vacciner”Hvis vi vil være i stand til at levere mRNA, så har vi brug for en mekanisme til at være mere effektiv til det, fordi alt, hvad der har været brugt indtil nu, giver dig en meget lille brøkdel af, hva
- Bluetooth -klistermærker på dit tøj? Startup Wiliot får $20 millioner for sporingsteknologi
- Taber valget? Hvem skal man bebrejde?
- Undersøgelse finder, at online restaurantinformation kan forudsige vigtige nabolagsindikatorer
- Hvorfor er oxidationstallet for S i FeS2 -1?
- En ingeniør foreslår en ny model for måden, hvorpå mennesker lokaliserer lyde
- Forskere rangerer de smarteste fiskestimer, når det kommer til rejseformationer


