Hvis halogenatomer erstattede brint i molekylerne, ville geometri af forandring?
* Elektronegativitet: Halogener er meget mere elektronegativ end brint. Dette betyder, at de tiltrækker elektroner stærkere, hvilket fører til en ændring i elektronfordelingen i molekylet.
* obligationslængde og vinkel: Halogenatomer er større end hydrogenatomer. Dette resulterer i længere bindinger og potentielt ændrede bindingsvinkler, der påvirker molekylets samlede form.
* Ensomme par: Halogenatomer har flere ensomme par elektroner end brint. Disse ensomme par kan afvise bindingspar, hvilket yderligere påvirker bindingsvinkler og molekylær geometri.
Eksempler:
* methan (CH4) vs. chlormethan (CH3CL): Metan er tetrahedral med alle bindingsvinkler ved 109,5 °. Når et brint erstattes af klor, bliver molekylet let forvrænget på grund af elektronegativitetsforskellen og den større størrelse af klor. Bindingsvinklen mellem kulstof og kloratom vil være lidt mindre end 109,5 °.
* vand (H2O) mod brintfluorid (HF): Vand har en bøjet form på grund af de ensomme par på ilt. Udskiftning af et brint med fluor gør molekylet endnu mere polært og ændrer bindingsvinklen lidt.
* ammoniak (NH3) vs. chloramin (NH2CL): Ammoniak har en trigonal pyramidal form på grund af det ensomme par på nitrogen. Udskiftning af et brint med klor ændrer geometrien markant, hvilket gør det mere polært og potentielt skifter bindingsvinklerne.
Kortfattet:
Udskiftningen af hydrogenatomer med halogenatomer i et molekyle kan væsentligt påvirke dens geometri på grund af faktorer som elektronegativitet, bindingslængde, bindingsvinkler og tilstedeværelsen af ensomme par. De specifikke ændringer afhænger af det specifikke molekyle og det involverede halogen.
Sidste artikelNår gasformige molekyler komprimeres, har de en tendens til?
Næste artikelHvilken blanding gør den bedste bobleopløsning?
 Varme artikler
Varme artikler
-
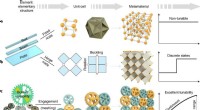 Gear-baserede mekaniske metamaterialer giver mulighed for oprettelse af konfigurerbare arkDesignkoncepter af mekaniske metamaterialer. a,b, klassisk paradigme:ikke-afstembart metamateriale (a) og typisk rekonfigurerbart metamateriale (b). c, Gear-baserede metamaterialer. Kredit:Nature Mate
Gear-baserede mekaniske metamaterialer giver mulighed for oprettelse af konfigurerbare arkDesignkoncepter af mekaniske metamaterialer. a,b, klassisk paradigme:ikke-afstembart metamateriale (a) og typisk rekonfigurerbart metamateriale (b). c, Gear-baserede metamaterialer. Kredit:Nature Mate -
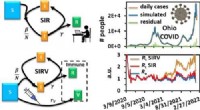 Kemi-laboratoriestuderende forudsiger spredning af COVID-19 med kinetikmodellerI denne graf forudsagde studerende i forårets kinetiklaboratorium daglige tilfælde i staten Ohio til efteråret 2022. Kredit:Ohio University Kemiker Jixin Chen så på den hurtige spredning af COVID-1
Kemi-laboratoriestuderende forudsiger spredning af COVID-19 med kinetikmodellerI denne graf forudsagde studerende i forårets kinetiklaboratorium daglige tilfælde i staten Ohio til efteråret 2022. Kredit:Ohio University Kemiker Jixin Chen så på den hurtige spredning af COVID-1 -
 Nye ultra-resistente og selvreparerende betonmaterialerKredit:Universitat Politècnica de València Et team fra Universitat Politècnica de València (UPV) og Politecnico di Milano har designet nye ultra-resistente og selvreparerende betonmaterialer. De h
Nye ultra-resistente og selvreparerende betonmaterialerKredit:Universitat Politècnica de València Et team fra Universitat Politècnica de València (UPV) og Politecnico di Milano har designet nye ultra-resistente og selvreparerende betonmaterialer. De h -
 Forskere foreslår en ny metode til at syntetisere et lovende magnetisk materialeMikrofotografering af Dy3Fe5O12. Kredit:Svetlana Saikova Forskere fra Siberian Federal University (SFU) og Det Russiske Videnskabsakademi har brugt en ny metode til at syntetisere jern-dysprosium
Forskere foreslår en ny metode til at syntetisere et lovende magnetisk materialeMikrofotografering af Dy3Fe5O12. Kredit:Svetlana Saikova Forskere fra Siberian Federal University (SFU) og Det Russiske Videnskabsakademi har brugt en ny metode til at syntetisere jern-dysprosium
- Hvor mange CM er der i en telefon?
- Hvad er netneutralitet, og hvorfor betyder det noget?
- Tager de vitale tegn på det globale hav med biogeokemiske flyder
- Ny undersøgelse bekræfter bølget arkproteinstruktur forudsagt i 1953
- Kan fritidsidræt virkelig gøre dig til en bedre studerende?
- Skolefravær har overraskende konsekvenser for voksne


