Hvor mange elektroner har magnesium brug for at tabe en fuld ydre skal?
Her er hvorfor:
* Magnesiums elektronkonfiguration: Magnesium har 12 elektroner med konfigurationen 2-8-2. Dette betyder, at det har 2 elektroner i sin yderste skal (den 3. skal).
* fuld ydre skal: En fuld ydre skal til magnesium ville være 8 elektroner (som den ædle gas neon).
* taber elektroner: Magnesium kan opnå en fuld ydre skal ved at miste sine 2 ydre elektroner, hvilket efterlader det med en stabil konfiguration af 2-8.
Denne proces med at miste elektroner gør magnesium A positivt ladet ion (Mg²⁺).
 Varme artikler
Varme artikler
-
 Fra gerningsstedet til retssalen - en DNA -prøves rejsePolitiet skal sikre, at prøver ikke er forurenet. Kredit:James Hereward og Caitlin Curtis, Forfatter angivet O.J. Simpson-mordssagen i 1995 introducerede DNA-kriminalteknik for offentligheden. Sag
Fra gerningsstedet til retssalen - en DNA -prøves rejsePolitiet skal sikre, at prøver ikke er forurenet. Kredit:James Hereward og Caitlin Curtis, Forfatter angivet O.J. Simpson-mordssagen i 1995 introducerede DNA-kriminalteknik for offentligheden. Sag -
 Effektivt materiale udviklet til at forhindre post-kirurgisk vedhæftning(a) De levende celler uden for 1 μL prikken i PEC angiver, at materialet ikke skaber et giftigt miljø (målestreg:500 μm). Dette tyder på, at materialet hæmmer levedygtighed, når celler er knyttet dire
Effektivt materiale udviklet til at forhindre post-kirurgisk vedhæftning(a) De levende celler uden for 1 μL prikken i PEC angiver, at materialet ikke skaber et giftigt miljø (målestreg:500 μm). Dette tyder på, at materialet hæmmer levedygtighed, når celler er knyttet dire -
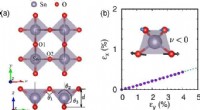 Forskere laver teoretisk forudsigelse af 2-D halvleder tindioxidFig. 1. (a) Atomstrukturen af et 2D δ-SnO2-monolag. (b) Stammen i x -retningen som følge af en påført trækbelastning i y -retningen. Kredit:JIANG Peng For nylig, Prof. 2 ) enkeltlagsfase (P-4
Forskere laver teoretisk forudsigelse af 2-D halvleder tindioxidFig. 1. (a) Atomstrukturen af et 2D δ-SnO2-monolag. (b) Stammen i x -retningen som følge af en påført trækbelastning i y -retningen. Kredit:JIANG Peng For nylig, Prof. 2 ) enkeltlagsfase (P-4 -
 Forskere skaber syntetisk prototissue, der kan synkroniseresOpdagelsen, udgivet i Naturmaterialer , er den første kemisk programmerede tilgang til fremstilling af et kunstigt væv. Fundene, som kan have store sundhedsmæssige anvendelser i fremtiden, kunne se
Forskere skaber syntetisk prototissue, der kan synkroniseresOpdagelsen, udgivet i Naturmaterialer , er den første kemisk programmerede tilgang til fremstilling af et kunstigt væv. Fundene, som kan have store sundhedsmæssige anvendelser i fremtiden, kunne se
- Fordele og ulemper ved at reflektere teleskoper
- Volvos Polestar åbner Kina-fabrik for at eksportere til Europa, OS
- Tre hydroxidioner er nødvendige for at danne en neutral ionforbindelse med en aluminiumion?
- Luftkvaliteten på mange togstationer er alarmerende dårlig - her er, hvordan du forbedrer den
- Bloomberg donerer 64 millioner dollars til at bekæmpe Trumps kuldagsorden
- Første indtryk kan påvirke finansielle fagfolks prognoser for virksomheder i op til 6 år


