Hvordan ved vi, at grafit er et metal?
Her er hvorfor:
* Elektrisk ledningsevne: Mens grafit udfører elektricitet, gør det det anderledes end metaller. Metaller udfører elektricitet gennem et "hav" af frie elektroner, mens Graphit's ledningsevne skyldes de delokaliserede elektroner i dens lagdelte struktur.
* Luster: Grafit har en kedelig, grålig udseende, i modsætning til den skinnende glans af metaller.
* formbarhed og duktilitet: Grafit er sprød og kan let brydes, i modsætning til metaller, der er formbare (kan hamres i ark) og duktile (kan trækkes ind i ledninger).
* Kemiske egenskaber: Grafit er kemisk inert og resistent over for korrosion, i modsætning til mange metaller, der let reagerer med syrer og andre kemikalier.
Grafit klassificeres faktisk som en metalloid , undertiden benævnt en semimetal . Metalloider har egenskaber for både metaller og ikke -metaller, og grafit udviser denne dualitet i dens ledningsevne og andre egenskaber.
 Varme artikler
Varme artikler
-
 Forskere foreslår at bruge pindsvin-lignende partikler til at fremskynde cellebiokemiske reaktionerUrchin-lignende partikler rettet af et magnetfelt. Kredit:Dmitry Lisovsky Forskning fra ITMO foreslår at bruge urchin-lignende partikler styret af et magnetfelt til at fremskynde kemiske reaktione
Forskere foreslår at bruge pindsvin-lignende partikler til at fremskynde cellebiokemiske reaktionerUrchin-lignende partikler rettet af et magnetfelt. Kredit:Dmitry Lisovsky Forskning fra ITMO foreslår at bruge urchin-lignende partikler styret af et magnetfelt til at fremskynde kemiske reaktione -
 Bedre forståelse af principperne for siliciumætsning fører til forbedret overflademønsterVed hjælp af nøje udvalgte kombinationer af metaller, det er muligt at etse indviklede mønstre på en siliciumoverflade, som vist ovenfor. Kredit:Ref. 1 og licenseret under CC BY 4.0 © 2016 L. Kong et
Bedre forståelse af principperne for siliciumætsning fører til forbedret overflademønsterVed hjælp af nøje udvalgte kombinationer af metaller, det er muligt at etse indviklede mønstre på en siliciumoverflade, som vist ovenfor. Kredit:Ref. 1 og licenseret under CC BY 4.0 © 2016 L. Kong et -
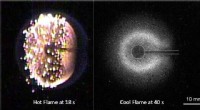 Seje flammer antændte i rummetVarme flammer (venstre) viger for kølige flammer (højre). Kredit:University of Maryland En opdagelse er blevet gjort i Jordens kredsløb - konstante sfæriske kølige diffusionsflammer. Målinger i di
Seje flammer antændte i rummetVarme flammer (venstre) viger for kølige flammer (højre). Kredit:University of Maryland En opdagelse er blevet gjort i Jordens kredsløb - konstante sfæriske kølige diffusionsflammer. Målinger i di -
 Forskere elektrificerer aluminium for at fremskynde vigtig procesEn ny undersøgelse viser, at en vigtig kemisk omdannelse, der bruges til at fremstille lægemidler, gødning og andre ting kan opnås hurtigere og billigere ved hjælp af elektricitet og aluminium. Kredit
Forskere elektrificerer aluminium for at fremskynde vigtig procesEn ny undersøgelse viser, at en vigtig kemisk omdannelse, der bruges til at fremstille lægemidler, gødning og andre ting kan opnås hurtigere og billigere ved hjælp af elektricitet og aluminium. Kredit
- Forskellen mellem Sole & Flounder
- Bedre dig end mig, Trump fortæller rekordstore astronaut
- Folk kan støtte klimaindsats stærkere, hvis de forstår, hvordan deres helbred er i fare
- Forskere opdager, at et enkelt lag af bittesmå diamanter øger elektronemissionen 13, 000 gange
- Hvorfor holder du dit hus så koldt? Undersøgelse tyder på, at temperaturen i barndommens hjem kan…
- Suomi NPP -satellit giver rigelige oplysninger om brande i Californien


