Et tal foran en kemisk formel en ligning, der angiver, hvor mange molekyler eller atomer hver reaktant og produkt er involveret reaktion?
Her er en sammenbrud:
* støkiometri er undersøgelsen af de kvantitative forhold mellem reaktanter og produkter i kemiske reaktioner.
* støkiometriske koefficienter er tallene placeret foran kemiske formler i en afbalanceret kemisk ligning.
* De repræsenterer det relative antal mol af hver reaktant og produkt involveret i reaktionen.
Eksempel:
Den afbalancerede kemiske ligning for forbrænding af metan er:
Ch₄ + 2o₂ → CO₂ + 2H₂O
* Koefficienten 1 Foran ch₄ indikerer, at en mol metan reagerer.
* Koefficienten 2 Foran O₂ indikerer, at der kræves to mol ilt.
* Koefficienten 1 Foran CO₂ indikerer, at der produceres en mol kuldioxid.
* Koefficienten 2 Foran H₂O indikerer, at der produceres to mol vand.
Nøglepunkter:
* Støkiometriske koefficienter er afgørende for at afbalancere kemiske ligninger, hvilket sikrer, at antallet af atomer i hvert element er det samme på begge sider af ligningen.
* De giver information om de relative mængder reaktanter og produkter, der er involveret i en reaktion.
* De kan bruges til at beregne mængden af reaktanter eller de nødvendige produkter eller produceres i en given reaktion.
Sidste artikelHvorfor reagerer ikke -metaller ikke med vand, mens de gør?
Næste artikelHvad er Beryllium massenummer?
 Varme artikler
Varme artikler
-
 Modificeret bakterie omdanner petroleum direkte til byggesten til plastKredit:Wageningen UR En bakterie opfylder et længe næret ønske fra mange kemikere. E. coli bakterien, som er blevet modificeret for at udstyre den med specielle enzymer, har vist sig at lave bygge
Modificeret bakterie omdanner petroleum direkte til byggesten til plastKredit:Wageningen UR En bakterie opfylder et længe næret ønske fra mange kemikere. E. coli bakterien, som er blevet modificeret for at udstyre den med specielle enzymer, har vist sig at lave bygge -
 Effektiv syntese af ginkgo -forbindelse kan føre til nye lægemidler, grønne insekticiderKredit:Scripps Kemikere ved Scripps Research har opfundet en effektiv metode til fremstilling af en syntetisk version af planteforbindelsen bilobalid, som naturligt produceres af gingkotræer. Det
Effektiv syntese af ginkgo -forbindelse kan føre til nye lægemidler, grønne insekticiderKredit:Scripps Kemikere ved Scripps Research har opfundet en effektiv metode til fremstilling af en syntetisk version af planteforbindelsen bilobalid, som naturligt produceres af gingkotræer. Det -
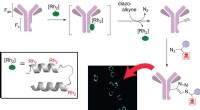 Metal forenkler syntesen af antistoflægemidlerRice University-kemikere har designet et plug-in metalloprotein for at forenkle opgaven med at lave målrettede antistofterapier. Forskerne brugte et tredobbeltmetaliseret peptid (indsat) til at give e
Metal forenkler syntesen af antistoflægemidlerRice University-kemikere har designet et plug-in metalloprotein for at forenkle opgaven med at lave målrettede antistofterapier. Forskerne brugte et tredobbeltmetaliseret peptid (indsat) til at give e -
 Kunstig receptor skelner mellem mandlige og kvindelige hormonerEn skematisk fremstilling af den selektive binding af testosteron fra en blanding af testosteron, progesteron, og beta-østradiol i vand. Receptoren har et indre hulrum med en diameter på cirka en nano
Kunstig receptor skelner mellem mandlige og kvindelige hormonerEn skematisk fremstilling af den selektive binding af testosteron fra en blanding af testosteron, progesteron, og beta-østradiol i vand. Receptoren har et indre hulrum med en diameter på cirka en nano
- Hvordan virker en kalorimeter?
- Bioinspirerede elektromekaniske nanogeneratorer til at regulere celleaktivitet
- Hvad er polariteten af natriumbenzoat?
- Forskning finder, at virkningen af tornadoskader kan tredobles i slutningen af det 21. århundre…
- Rekordbrækkende metalens kunne revolutionere optiske teknologier
- Flade ansigter og vejrtrækningsbesvær:Hvordan kæledyrstendenser har skadet dyresundheden - og hva…


