Hvilket volumen er nødvendigt for at opbevare 0,08 mol heliumgas ved 204,67 kp og 300 K?
1. Den ideelle gaslov
Den ideelle gaslov er:
PV =NRT
Hvor:
* P =pres (i Pascals)
* V =volumen (i kubikmeter)
* n =antal mol
* R =ideel gaskonstant (8.314 j/mol · k)
* T =temperatur (i Kelvin)
2. Konverter enheder
* tryk: Konverter KPA til Pascals:204,67 KPa * 1000 PA/KPA =204670 PA
3. Omarranger den ideelle gaslov til at løse for volumen (v)
V =(nrt) / p
4. Tilslut værdierne
V =(0,08 mol * 8,314 J / mol · K * 300 K) / 204670 PA
5. Beregn lydstyrken
V ≈ 0,00097 m³
6. Konverter til en mere praktisk enhed
* kubikmeter til liter: 0,00097 m³ * 1000 l/m³ ≈ 0,97 l
Derfor har du brug for ca. 0,97 liter for at opbevare 0,08 mol heliumgas ved 204,67 kPa og 300 K.
Sidste artikelHvilke af disse fik navnet Pangea?
Næste artikelHvad er navnet på salt, der er til stede i lysende maling?
 Varme artikler
Varme artikler
-
 Ny tekstilfarvningsmetode reducerer drastisk vandbehov og giftig udledning af farvestoffer drastiskAnuradhi Liyanapathiranage er ph.d. kandidat i College of Family and Consumer Sciences. Kredit:Nancy Evelyn/UGA Anuradhi Liyanapathiranage brænder for bæredygtighed og beskyttelse af miljøet genne
Ny tekstilfarvningsmetode reducerer drastisk vandbehov og giftig udledning af farvestoffer drastiskAnuradhi Liyanapathiranage er ph.d. kandidat i College of Family and Consumer Sciences. Kredit:Nancy Evelyn/UGA Anuradhi Liyanapathiranage brænder for bæredygtighed og beskyttelse af miljøet genne -
 Den næste store ting:Hvordan bringer videnskabsmænd brintbrændselsceller fra laboratoriet til det…Skematisk illustration af den syntetiske metode til højtemperatursvovlforankring. Kredit:USTC Brændselsceller vinder på grund af deres høje effektivitet og miljøvenlige egenskaber i processen med e
Den næste store ting:Hvordan bringer videnskabsmænd brintbrændselsceller fra laboratoriet til det…Skematisk illustration af den syntetiske metode til højtemperatursvovlforankring. Kredit:USTC Brændselsceller vinder på grund af deres høje effektivitet og miljøvenlige egenskaber i processen med e -
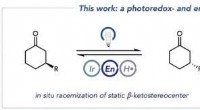 Forskere rapporterer om ny platform for stereokontrolDen overordnede transformation, der kombinerer racemisering af ketonsubstraterne (til venstre) med biokatalytisk reduktion til enantiomert rene alkoholprodukter (i midten), og den vigtigste enaminylra
Forskere rapporterer om ny platform for stereokontrolDen overordnede transformation, der kombinerer racemisering af ketonsubstraterne (til venstre) med biokatalytisk reduktion til enantiomert rene alkoholprodukter (i midten), og den vigtigste enaminylra -
 Konkylieskaller spreder hemmeligheden bag deres sejhedTeamet 3-D printede kompositmaterialer med præcist kontrollerede strukturer, og udførte test i et faldtårn, der gjorde det muligt for dem at observere præcis, hvordan revner opstod og spredte sig - el
Konkylieskaller spreder hemmeligheden bag deres sejhedTeamet 3-D printede kompositmaterialer med præcist kontrollerede strukturer, og udførte test i et faldtårn, der gjorde det muligt for dem at observere præcis, hvordan revner opstod og spredte sig - el
- Oversvømmelser fra rester af tropisk storm fanger Phoenix-biler
- Hvad bruges ATP kaldet?
- Vinteren starter for sent i normalt kølige landdistrikter i Alaska
- Twitter, Facebook forbyder falske brugere; nogle havde AI-skabte billeder
- Microsoft konkurrerer om popularitet med upstart Slack
- Træning af computere til at genkende dynamiske hændelser


