Hvilke bindinger udøver begge atomer det samme træk på delte elektroner?
Her er hvorfor:
* kovalent binding: I en kovalent binding deler atomer elektroner for at opnå en stabil elektronkonfiguration.
* Polaritet: Electronegativity af et atom (dens evne til at tiltrække elektroner) bestemmer, hvor stærkt det trækker på delte elektroner.
* ikke -polær: Når to atomer har den samme elektronegativitet, trækker de på de delte elektroner med lige kraft. Dette resulterer i en afbalanceret fordeling af elektrondensitet og en ikke -polær binding.
Eksempel: Et molekyle af ilt (O 2 ) har en ikke -polær kovalent binding, fordi begge iltatomer har den samme elektronegativitet.
Sidste artikelHvilke atomer kan danne H -bindinger?
Næste artikelHvad er crenellations for?
 Varme artikler
Varme artikler
-
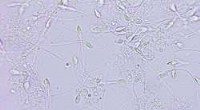 Forskere udvikler en ny clip-on-enhed til smartphones til analyse af sædcellerKredit:Lukasz Pawel Szczepanski, Shutterstock Mandlig infertilitetstest udføres i øjeblikket udelukkende i laboratorier, kræver flere besøg og flere dage for at få et resultat. Det EU-finansierede
Forskere udvikler en ny clip-on-enhed til smartphones til analyse af sædcellerKredit:Lukasz Pawel Szczepanski, Shutterstock Mandlig infertilitetstest udføres i øjeblikket udelukkende i laboratorier, kræver flere besøg og flere dage for at få et resultat. Det EU-finansierede -
 Grafen øger perovskite-enkeltkrystal-fotodetektorens ydeevneKredit:CC0 Public Domain På grund af den brede anvendelse af fotodetektorer inden for områder, herunder optisk kommunikation, miljøovervågning, og billedsansning, forskning i udvikling af højeffek
Grafen øger perovskite-enkeltkrystal-fotodetektorens ydeevneKredit:CC0 Public Domain På grund af den brede anvendelse af fotodetektorer inden for områder, herunder optisk kommunikation, miljøovervågning, og billedsansning, forskning i udvikling af højeffek -
 Kampen mod huller i tænderne får hjælp til et nyt smart materialeProfessor Ben Hatton ved University of Toronto, Professor Yoav Finer og ph.d.-kandidat Cameron Stewart. Kredit:Yodit Tedla/Tandlægefakultetet. Når patienter går til tandlægen for at fylde et hulru
Kampen mod huller i tænderne får hjælp til et nyt smart materialeProfessor Ben Hatton ved University of Toronto, Professor Yoav Finer og ph.d.-kandidat Cameron Stewart. Kredit:Yodit Tedla/Tandlægefakultetet. Når patienter går til tandlægen for at fylde et hulru -
 Giftforskning kan give behandling af mave-tarmsygdommeTerapeutik inspireret af gifte kan være nøglen til behandling af en almindelig mave-tarmsygdom. Kredit:University of Queensland Terapeutik inspireret af gifte kan være nøglen til behandling af en
Giftforskning kan give behandling af mave-tarmsygdommeTerapeutik inspireret af gifte kan være nøglen til behandling af en almindelig mave-tarmsygdom. Kredit:University of Queensland Terapeutik inspireret af gifte kan være nøglen til behandling af en
- Skovbrande fejer ind i parken i Brasilien, der huser jaguarer
- Periodisk gennemgang af kunstig intelligens-industrien afslører udfordringer
- Klimaforandringer i balancen
- Rørkort omkring planeter og måner muliggjort af knudeteori
- GPM satellit analyserer den tropiske cyklon Fehis nedbør
- Værktøjer, der bruges til at måle orkaner


