Hvordan forbliver en forbindelse sammen?
Her er de vigtigste typer kemiske bindinger:
* ioniske bindinger: Dannet, når en eller flere elektroner overføres fra et atom til et andet, hvilket resulterer i positivt og negativt ladede ioner, der tiltrækker hinanden. Dette ses ofte i forbindelser dannet mellem metaller og ikke -metaller.
* kovalente obligationer: Dannet, når atomer deler elektroner. Dette forekommer mellem ikke -metaller, og de delte elektroner tiltrækkes af kernerne i begge atomer og holder dem sammen.
* Metalliske obligationer: Dannet, når metalatomer deler deres valenselektroner i et "hav af elektroner". Dette gør det muligt for elektronerne at bevæge sig frit gennem metallet, hvilket giver det sine karakteristiske egenskaber som ledningsevne og formbarhed.
styrken af disse bindinger bestemmer, hvor stabil en forbindelse er. Stærkere bindinger betyder, at en forbindelse er mindre tilbøjelig til at bryde fra hinanden.
Andre faktorer, der bidrager til stabiliteten af en forbindelse, inkluderer:
* Elektronegativitet: Et atomens tendens til at tiltrække elektroner i en binding. En stor forskel i elektronegativitet mellem atomer fører til flere polære bindinger, som er stærkere.
* molekylær geometri: Arrangementet af atomer i et molekyle. Dette kan påvirke fordelingen af elektroner og styrken af intermolekylære kræfter.
* Intermolekylære kræfter: Dette er svagere attraktioner mellem molekyler, såsom hydrogenbinding, dipol-dipolinteraktioner og London-spredningskræfter. De spiller en rolle i de fysiske egenskaber ved en forbindelse, som kogepunkt og smeltepunkt.
Sammenfattende forbliver en forbindelse sammen på grund af de attraktive kræfter mellem dens atomer, primært gennem kemiske bindinger. Styrken og arten af disse bindinger sammen med andre faktorer som elektronegativitet og molekylær geometri, bestem forbindelsens stabilitet og egenskaber.
 Varme artikler
Varme artikler
-
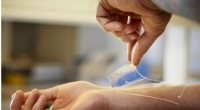 Nyt materiale til behandling af sår kan beskytte mod resistente bakterierForskere ved Chalmers Tekniske Universitet, Sverige, har udviklet et nyt materiale, der dræber bakterier og potentielt kan forhindre infektioner i sår - en specialdesignet hydrogel, der virker mod all
Nyt materiale til behandling af sår kan beskytte mod resistente bakterierForskere ved Chalmers Tekniske Universitet, Sverige, har udviklet et nyt materiale, der dræber bakterier og potentielt kan forhindre infektioner i sår - en specialdesignet hydrogel, der virker mod all -
 Forskere udvikler faseændringshukommelsesenheder til mere kraftfuld computingEt samarbejde mellem laboratoriet af Judy Cha, Carol og Douglas Melamed adjunkt i maskinteknik og materialevidenskab, og IBMs Watson Research Center kunne hjælpe med at gøre en potentielt revolutioner
Forskere udvikler faseændringshukommelsesenheder til mere kraftfuld computingEt samarbejde mellem laboratoriet af Judy Cha, Carol og Douglas Melamed adjunkt i maskinteknik og materialevidenskab, og IBMs Watson Research Center kunne hjælpe med at gøre en potentielt revolutioner -
 Forskere udvikler miljøvenlig pollensvamp til at håndtere vandforureningerFor at lave svampen, forskergruppen omdannede først hårde pollenkorn til et blødt gelignende materiale, inden frysetørring af materialet. Disse processer resulterede i dannelsen af pollensvampe med
Forskere udvikler miljøvenlig pollensvamp til at håndtere vandforureningerFor at lave svampen, forskergruppen omdannede først hårde pollenkorn til et blødt gelignende materiale, inden frysetørring af materialet. Disse processer resulterede i dannelsen af pollensvampe med -
 Meget effektiv enkeltatom-katalysator kan hjælpe bilindustrienSingle-atom platin (blå kugle) belagt guld (gul kugle) nanopartikler kan tjene som en yderst effektiv katalysator for en brændselscelle kemisk reaktion (dvs. myresyreoxidation). Kredit:Canadian Light
Meget effektiv enkeltatom-katalysator kan hjælpe bilindustrienSingle-atom platin (blå kugle) belagt guld (gul kugle) nanopartikler kan tjene som en yderst effektiv katalysator for en brændselscelle kemisk reaktion (dvs. myresyreoxidation). Kredit:Canadian Light
- Sjældent boomerang-jordskælv observeret langs Atlanterhavets forkastningslinje
- Undersøgelse viser, at smitte kan være katalysatorer for massemigration
- NASA dækker naturbrande fra mange kilder
- Hvad skal være sandt om den nettoioniske ladning i en forbindelse?
- Ny forskning viser hydrologiske grænser i kulstoffangst og -lagring
- Solbrint:Lad os overveje stabiliteten af fotoelektroder


