Hvorfor forekommer smeltning af is?
1. Molekylær struktur:
* Is er en solid form for vand, hvor vandmolekyler er arrangeret i en stiv, krystallinsk struktur, der holdes sammen af stærke brintbindinger.
* Disse bindinger begrænser molekylernes bevægelse.
2. Varmeenergi og molekylær bevægelse:
* Når varmeenergi påføres is, absorberes den af vandmolekylerne.
* Denne absorberede energi øger molekylernes vibrations- og rotationsbevægelse.
3. Breaking Bonds:
* Når den molekylære bevægelse øges, svækkes brintbindingerne, der holder strukturen sammen og til sidst går i stykker.
* Dette forstyrrer den stive krystallinske isstruktur.
4. Overgang til væske:
* Med de knækkede bindinger får molekylerne mere frihed til at bevæge sig rundt.
* De bliver nærmere fordelt og forstyrrede og skifter fra fast tilstand til flydende tilstand (vand).
5. Smeltepunkt:
* Temperaturen, hvorpå is smelter, kaldes smeltepunktet (0 ° C eller 32 ° F).
* Ved denne temperatur er den leverede varmeenergi tilstrækkelig til at overvinde de attraktive kræfter mellem vandmolekylerne og bryde den krystallinske struktur.
I det væsentlige er smeltning en faseovergang, hvor absorptionen af varmeenergi øger den molekylære bevægelse af vandmolekyler, bryder de bindinger, der holder dem i en fast tilstand og giver dem mulighed for at flyde frit som en væske.
Sidste artikelHvorfor går ibrudt metaller?
Næste artikel15.Hvorfor har en mol carbonatomer en mindre masse end svovlatomer?
 Varme artikler
Varme artikler
-
 Pandemisk forebyggelse i lufthavneIsabel Steppert, videnskabsmand ved Fraunhofer IZI, under prøvemåling. Kredit:Fraunhofer IZI Globale flyrejser er ikke begrænset til mennesker og varer - smitsomme agenter, også, kan lægge vejen o
Pandemisk forebyggelse i lufthavneIsabel Steppert, videnskabsmand ved Fraunhofer IZI, under prøvemåling. Kredit:Fraunhofer IZI Globale flyrejser er ikke begrænset til mennesker og varer - smitsomme agenter, også, kan lægge vejen o -
 Næste generations opløsningsmidler fanger kulstof med halvdelen af energienPacific Northwest National Laboratory -videnskabsmand David Heldebrant fanger svovl og kuldioxid fra testemissionsstrømme i en proces kaldet Reversible Acid Gas Capture. Kredit:Pacific Northwest Natio
Næste generations opløsningsmidler fanger kulstof med halvdelen af energienPacific Northwest National Laboratory -videnskabsmand David Heldebrant fanger svovl og kuldioxid fra testemissionsstrømme i en proces kaldet Reversible Acid Gas Capture. Kredit:Pacific Northwest Natio -
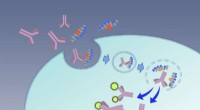 Særlig levering:Makromolekyler via edderkopper biderForskere ombygger edderkoppegift, så endosomer kan levere sin last mere effektivt i cellerne. Kredit:Kyoto University Vores celler er rige på proteiner, som er potentielle mål for terapi. Men unde
Særlig levering:Makromolekyler via edderkopper biderForskere ombygger edderkoppegift, så endosomer kan levere sin last mere effektivt i cellerne. Kredit:Kyoto University Vores celler er rige på proteiner, som er potentielle mål for terapi. Men unde -
 Forskere bygger første deployable, gå, blød robotIllustration af DeployBots, der installerer sig selv på en planet for at udforske rummet. Kredit:Wang et al. ©2017 Royal Society of Chemistry (Phys.org)—Forskere har bygget den første robot lavet
Forskere bygger første deployable, gå, blød robotIllustration af DeployBots, der installerer sig selv på en planet for at udforske rummet. Kredit:Wang et al. ©2017 Royal Society of Chemistry (Phys.org)—Forskere har bygget den første robot lavet
- Kampen mod huller i tænderne får hjælp til et nyt smart materiale
- Astronomer undersøger stjernedannende processer i det unge stjerneobjekt G29.862–0.044
- Hvad fortæller Google-søgninger os om vores frygt for klimaændringer?
- Dig tager et kig på, hvordan New Hampshire Shakers interagerede
- Fortnite lærer de forkerte lektioner
- Hvem hopper de længste Robert på 4 meter eller James 12 meter?


