Hvilket er blødeste natrium eller lithium?
Forklaring:
* Metallisk binding: Både lithium og natrium er alkalimetaller, og deres blødhed skyldes deres svage metalliske binding.
* atomstørrelse: Lithium har en mindre atomradius end natrium. Dette betyder, at lithiumatomerne er tættere sammen i det metalliske gitter, hvilket resulterer i svagere metalliske bindinger.
* Elektropositivitet: Lithium er mere elektropositiv end natrium, hvilket betyder, at det har en større tendens til at miste elektroner. Dette svækker yderligere den metalliske binding i lithium.
På grund af sin mindre atomstørrelse og højere elektropositivitet har lithium derfor svagere metalliske bindinger og er blødere end natrium.
 Varme artikler
Varme artikler
-
 Kontrol af membranernes nanoskala struktur er nøglen til rent vand, finder forskereKredit:Pixabay/CC0 Public Domain En afsaltningsmembran fungerer som et filter til saltvand:Skub vandet gennem membranen, få rent vand egnet til landbrug, energiproduktion og endda drikke. Processe
Kontrol af membranernes nanoskala struktur er nøglen til rent vand, finder forskereKredit:Pixabay/CC0 Public Domain En afsaltningsmembran fungerer som et filter til saltvand:Skub vandet gennem membranen, få rent vand egnet til landbrug, energiproduktion og endda drikke. Processe -
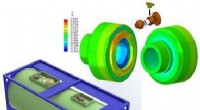 Matematisk model af termoplastisk komposit hjælper med at designe og certificere meget pålidelige …Kredit:Skolkovo Institut for Videnskab og Teknologi Forskere ved Skoltech Center for Design, Manufacturing and Materials og deres kolleger har udviklet og eksperimentelt verificeret modellen af
Matematisk model af termoplastisk komposit hjælper med at designe og certificere meget pålidelige …Kredit:Skolkovo Institut for Videnskab og Teknologi Forskere ved Skoltech Center for Design, Manufacturing and Materials og deres kolleger har udviklet og eksperimentelt verificeret modellen af -
 Baner vejen til kunstig fotosyntese:Effekt af doping på fotokatalysatoren SrTiO3Opladningsrekombination opstår, når mobile ladningsbærere til stede i materialet, der udsættes for lys, tilintetgør hinanden og kan hæmme fotokatalysatorens energieffektivitet. Kredit:Masashi Kato fra
Baner vejen til kunstig fotosyntese:Effekt af doping på fotokatalysatoren SrTiO3Opladningsrekombination opstår, når mobile ladningsbærere til stede i materialet, der udsættes for lys, tilintetgør hinanden og kan hæmme fotokatalysatorens energieffektivitet. Kredit:Masashi Kato fra -
 Reparation og regenerering af perifere nerver mulig med dobbelt polymer hydrogel klæbemiddelVævsteknik samler videnskabelige og medicinske eksperter inden for biomedicinsk teknik, materiale videnskab, molekylær og cellulær biologi, og genteknologi. Kredit:Mary Ann Liebert, Inc., forlag
Reparation og regenerering af perifere nerver mulig med dobbelt polymer hydrogel klæbemiddelVævsteknik samler videnskabelige og medicinske eksperter inden for biomedicinsk teknik, materiale videnskab, molekylær og cellulær biologi, og genteknologi. Kredit:Mary Ann Liebert, Inc., forlag
- Forskere undersøger adfærd i kvantesystemer med en legetøjsinspireret teknik
- Hvilket lag af jorden går vi altid på?
- Grækenlands første undervandsmuseum åbner den antikke verden for dykkerturister
- Molekylært stillads tilbyder nye tilgange til rygmarvsskade
- Sådan fungerer Virtual Reality
- Mobile kvinder var nøglen til kulturel udveksling i stenalderen og bronzealderens Europa


