Beskriv ændringen i reaktionshastigheden, når enzymkoncentrationen øges?
Her er hvorfor:
* enzymer er katalysatorer: De fremskynder reaktionerne ved at sænke aktiveringsenergien, men de forbruges ikke i processen. Dette betyder, at de kan bruges igen og igen.
* flere enzymer, mere aktive steder: Hvert enzymmolekyle har aktive steder, hvor underlag binder og reagerer. Forøgelse af enzymkoncentrationen betyder, at der er mere aktive steder, hvilket gør det muligt at behandle flere substratmolekyler samtidigt.
* øget kollisionsfrekvens: Med flere enzymmolekyler til stede, er der en større chance for, at substratmolekyler møder et aktivt sted, hvilket fører til hyppigere kollisioner og hurtigere reaktionshastigheder.
Imidlertid er dette forhold ikke lineært for evigt:
* Mætningspunkt: På et bestemt tidspunkt vil øge enzymkoncentrationen yderligere ikke øge reaktionshastigheden markant. Dette sker, når alle tilgængelige substratmolekyler er bundet til aktive steder, og enzymet bliver mættet.
* Andre begrænsende faktorer: Faktorer som substratkoncentration, temperatur og pH kan også begrænse reaktionshastigheden, uanset enzymkoncentration.
Kortfattet: Forøgelse af enzymkoncentration øger generelt reaktionshastigheden, men der er et mætningspunkt, hvor yderligere stigninger bliver mindre effektive.
Sidste artikelHvilken gas kan komprimeres og udvides?
Næste artikelHvad er molekylærformel for jod?
 Varme artikler
Varme artikler
-
 Aktiv camouflage kunstig hud i området synligt for infrarødtBlæksprutte enestående evne til at skjule sig i enhver baggrund har inspireret forskere til at gentage deres fascinerende evne til at camouflere i det infrarøde (IR) og synlige spektrum. Nylige fremsk
Aktiv camouflage kunstig hud i området synligt for infrarødtBlæksprutte enestående evne til at skjule sig i enhver baggrund har inspireret forskere til at gentage deres fascinerende evne til at camouflere i det infrarøde (IR) og synlige spektrum. Nylige fremsk -
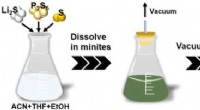 Udvikling af en ny storstilet fremstillingsteknologi til faste sulfidelektrolytterSkema af den nye løsningsbehandlingsteknologi for sulfid SEer. Kredit:Toyohashi University of Technology En forskergruppe i ph.d.-programmet ved Toyohashi University of Technologys afdeling for ele
Udvikling af en ny storstilet fremstillingsteknologi til faste sulfidelektrolytterSkema af den nye løsningsbehandlingsteknologi for sulfid SEer. Kredit:Toyohashi University of Technology En forskergruppe i ph.d.-programmet ved Toyohashi University of Technologys afdeling for ele -
 Forskere udvikler ny chip til hurtig og præcis sygdomsopdagelse til lave omkostningerNUS Engineering-forskere har udviklet en billig microfluid-chip, der hurtigt og præcist kan detektere og kvantificere nano-biopartikler ved hjælp af kun et standard laboratoriemikroskop uden fluoresce
Forskere udvikler ny chip til hurtig og præcis sygdomsopdagelse til lave omkostningerNUS Engineering-forskere har udviklet en billig microfluid-chip, der hurtigt og præcist kan detektere og kvantificere nano-biopartikler ved hjælp af kun et standard laboratoriemikroskop uden fluoresce -
 Forskere laver biologisk nedbrydelige mikroperler af celluloseDr. Janet Scott, Center for bæredygtige kemiske teknologier, University of Bath. Kredit:University of Bath Forskere og ingeniører fra University of Bath har udviklet bionedbrydelige cellulosemikro
Forskere laver biologisk nedbrydelige mikroperler af celluloseDr. Janet Scott, Center for bæredygtige kemiske teknologier, University of Bath. Kredit:University of Bath Forskere og ingeniører fra University of Bath har udviklet bionedbrydelige cellulosemikro
- Sørg for, at ESA'er sky- og aerosolsatellit er aerosolfri
- NA64 bruger højenergi SPS-myonstrålen til at søge efter mørkt stof
- Hvilke kemikalier forårsager afskum?
- Hot nikkel skubber grafen:Undersøgelse forenkler fremstilling af halvledende dobbeltlags grafen
- Hvor meget biomasse vokser der på savannen?
- Hvad er fem egenskaber ved gasser?


