Hvilken forbindelse har mindre end 8 elektroner?
* Octet -reglen: De fleste atomer stræber efter at have 8 elektroner i deres yderste skal (Valence Shell) for at opnå stabilitet. Dette kaldes Octet -reglen.
* Undtagelser: Der er nogle undtagelser fra Octet -reglen. Nogle elementer er tilfredse med færre end 8 elektroner i deres valensskal.
* Eksempler:
* brint (H): Det har kun brug for 2 elektroner for at fylde sin første skal.
* helium (He): Den har allerede 2 elektroner, hvilket gør sin første skal komplet.
* beryllium (BE): Det er stabilt med kun 4 elektroner i sin valensskal.
* bor (b): Det er stabilt med kun 6 elektroner i sin valensskal.
Vigtig note: Mens disse elementer * kan * eksistere som atomer med færre end 8 elektroner, findes de ofte i forbindelser, hvor de deler elektroner med andre atomer for at opnå en mere stabil konfiguration.
Fortæl mig, hvis du gerne vil gå dybere ned i ethvert specifikt element eller koncept!
Sidste artikelHvad viser de forskellige typer atomer?
Næste artikelHvilket element har 4 valenselektroner i den 6. skal?
 Varme artikler
Varme artikler
-
 Optrævling af historien og videnskaben bag gamle dekorative metaltrådeDette farvelagte mikroskopibillede af en 18 th århundredes metaltråd afslører, at den er lavet af et stykke metal viklet rundt om en silkekerne; indsat viser relative mængder af sølv og guld/sølv le
Optrævling af historien og videnskaben bag gamle dekorative metaltrådeDette farvelagte mikroskopibillede af en 18 th århundredes metaltråd afslører, at den er lavet af et stykke metal viklet rundt om en silkekerne; indsat viser relative mængder af sølv og guld/sølv le -
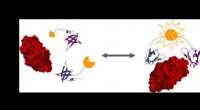 At bestemme, hvordan og hvorfor celler træffer beslutningerTo bindeproteiner (blå og lilla) er konstrueret til at binde et bestemt målprotein (rødt), såsom lysozym. Kun i nærvær af målproteinet samles de to halvdele af det delte luciferase-enzym (gul) for at
At bestemme, hvordan og hvorfor celler træffer beslutningerTo bindeproteiner (blå og lilla) er konstrueret til at binde et bestemt målprotein (rødt), såsom lysozym. Kun i nærvær af målproteinet samles de to halvdele af det delte luciferase-enzym (gul) for at -
 Ny måde at fremstille biomedicinsk udstyr på af silke giver bedre produkter med afstembare kvalite…Råprodukt i form af silkepulver kan nemt opbevares, transporteret, og støbt til forskellige former med overlegne egenskaber i forhold til mange andre materialer, der anvendes i medicinske implantater.
Ny måde at fremstille biomedicinsk udstyr på af silke giver bedre produkter med afstembare kvalite…Råprodukt i form af silkepulver kan nemt opbevares, transporteret, og støbt til forskellige former med overlegne egenskaber i forhold til mange andre materialer, der anvendes i medicinske implantater. -
 Ny enhed opdager hurtigt skadelige bakterier i blodetBakterieceller fanget i en 3D mikroperlematrix. Kredit:Wenrong He/Rochester Institute of Technology. Ingeniører har skabt en lillebitte enhed, der hurtigt kan opdage skadelige bakterier i blodet,
Ny enhed opdager hurtigt skadelige bakterier i blodetBakterieceller fanget i en 3D mikroperlematrix. Kredit:Wenrong He/Rochester Institute of Technology. Ingeniører har skabt en lillebitte enhed, der hurtigt kan opdage skadelige bakterier i blodet,
- Hvilken grad er et køleskab?
- Hvad er modgiften til kulilte?
- De Forenede Arabiske Emiraters Hope-sonde går ind i kredsløbet om Mars som den første for den ara…
- Sådan opretter du en enkel fjernbetjening Car
- Hvad er massen af 4,0 liter ilt?
- Kalorieindslag på menuer forårsager flere sundhedsomtaler i online restaurantanmeldelser


