Hvor mange mol gas er i beholder med et lukket har tryk 2,62 ATM -volumen 47,8 L og temperatur 775 K.?
den ideelle gaslov
Den ideelle gaslov er en grundlæggende ligning i kemi, der relaterer trykket (P), volumen (V), temperatur (T) og antal mol (N) af en ideel gas:
PV =NRT
Hvor:
* p =pres i atmosfærer (ATM)
* v =volumen i liter (L)
* n =antal mol
* r =Ideal gaskonstant (0,0821 L · ATM/Mol · K)
* t =temperatur i Kelvin (K)
Løsning for antallet af mol (n)
1.
n =pv / rt
2. Tilslut de givne værdier:
n =(2,62 atm) (47,8 l) / (0,0821 L · atm / mol · K) (775 K)
3. Beregn:
n ≈ 2,08 mol
Derfor er der ca. 2,08 mol gas i beholderen.
 Varme artikler
Varme artikler
-
 Billedteknologier øger fokus på gerningsstederKredit:European Cooperation in Science and Technology (COST) Kombinationen af flere billeder og banebrydende teknologi hjælper retsmedicin med at give retshåndhævende myndigheder, juryer og rets
Billedteknologier øger fokus på gerningsstederKredit:European Cooperation in Science and Technology (COST) Kombinationen af flere billeder og banebrydende teknologi hjælper retsmedicin med at give retshåndhævende myndigheder, juryer og rets -
 Ny familie af selektive sølvbaserede kræftbekæmpende lægemidler opdagetEn familie af økonomiske sølvbaserede komplekser viser meget lovende resultater mod en række menneskelige kræftformer i laboratorietest, med meget lav toksicitet i rotteundersøgelser og minimale virkn
Ny familie af selektive sølvbaserede kræftbekæmpende lægemidler opdagetEn familie af økonomiske sølvbaserede komplekser viser meget lovende resultater mod en række menneskelige kræftformer i laboratorietest, med meget lav toksicitet i rotteundersøgelser og minimale virkn -
 At bringe orden i kaotiske bobler kan gøre minedrift mere bæredygtigKredit:CC0 Public Domain En ny måde at kontrollere boblernes bevægelse på fra forskere ved Columbia Engineering kan en dag hjælpe med at adskille nyttige metaller fra ubrugeligt snavs ved at bruge
At bringe orden i kaotiske bobler kan gøre minedrift mere bæredygtigKredit:CC0 Public Domain En ny måde at kontrollere boblernes bevægelse på fra forskere ved Columbia Engineering kan en dag hjælpe med at adskille nyttige metaller fra ubrugeligt snavs ved at bruge -
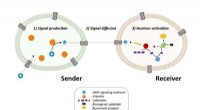 Livslignende celler kan nu kommunikere over lange afstande via signalforstærkningSkematisk over kommunikationen mellem to populationer af kunstige celler. Kredit:Bastiaan Buddingh Forskere har store drømme for kunstige celler. Disse replikaer af biologiske celler i laboratorie
Livslignende celler kan nu kommunikere over lange afstande via signalforstærkningSkematisk over kommunikationen mellem to populationer af kunstige celler. Kredit:Bastiaan Buddingh Forskere har store drømme for kunstige celler. Disse replikaer af biologiske celler i laboratorie
- Hvad mindede spiralgalaksen Hubble om?
- Bondings næste topmodel:Projektering af bindingsegenskaber med maskinlæring
- Undersøgelse kaster mere lys over karakteren af HESS J1857+026
- Sådan beregnes atmosfæretryk
- Har en asteroide en hale som en komet?
- Opdagelse af en hellig gral med opfindelsen af universel computerhukommelse


