Hvor mange subatomære partikler er der i guld?
Her er hvorfor:
* isotoper: Guld (AU) har flere isotoper, som er atomer med det samme element med det samme antal protoner, men forskellige antal neutroner. Den mest almindelige isotop er guld-197 (¹⁹⁷au) .
* Subatomære partikler: De tre vigtigste subatomære partikler er protoner, neutroner og elektroner.
* Protoner: Bestem elementet (guld har 79 protoner).
* neutroner: Varierer mellem isotoper. Gold -197 har 118 neutroner (197 - 79 =118).
* Elektroner: Normalt lig med antallet af protoner, så guld har 79 elektroner.
Derfor for den mest almindelige isotop, guld-197:
* Samlede subatomære partikler: 79 (protoner) + 118 (neutroner) + 79 (elektroner) = 276 subatomære partikler
Husk dog, at dette kun er til guld-197. Andre isotoper af guld vil have et andet antal neutroner og derfor et andet samlet antal subatomære partikler.
 Varme artikler
Varme artikler
-
 Silkeorme giver nyt spin på klæbrige molekylerTeamet har konstrueret silkeorme til at producere E-selectin, et kritisk adhæsionsmolekyle involveret i betændelse, kræft og andre sygdomsprocesser. Kredit:Takahiro Kusakabe &Jae Man Lee, Kyushu Unive
Silkeorme giver nyt spin på klæbrige molekylerTeamet har konstrueret silkeorme til at producere E-selectin, et kritisk adhæsionsmolekyle involveret i betændelse, kræft og andre sygdomsprocesser. Kredit:Takahiro Kusakabe &Jae Man Lee, Kyushu Unive -
 Forskere undersøger komplekse molekylære strukturerMolekylerne er blevet analyseret ved forskellige tryk (fra ultrahøjt vakuum til atmosfærisk tryk) Kredit:TU Wien Arbejdet med hæmoglobin ser ud til at være ret simpelt:Det transporterer iltmolekyl
Forskere undersøger komplekse molekylære strukturerMolekylerne er blevet analyseret ved forskellige tryk (fra ultrahøjt vakuum til atmosfærisk tryk) Kredit:TU Wien Arbejdet med hæmoglobin ser ud til at være ret simpelt:Det transporterer iltmolekyl -
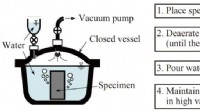 Udnytter slagfastheden i verdens hårdeste beton til katastrofeforebyggelseOversigt over afgasning og vandabsorberingsbehandling. PFC -prøverne placeres derefter i en lukket beholder, der blev trykløs ved hjælp af en vakuumpumpe, og vand indført fra den ydre overflade til in
Udnytter slagfastheden i verdens hårdeste beton til katastrofeforebyggelseOversigt over afgasning og vandabsorberingsbehandling. PFC -prøverne placeres derefter i en lukket beholder, der blev trykløs ved hjælp af en vakuumpumpe, og vand indført fra den ydre overflade til in -
 Forbedring af ydeevnen af metal-organiske rammematerialerMikrograffoto (samlet bredde ca. 1, 5 mm), der viser det nye adsorberende materiale, der blev fremstillet ved anvendelse af et poppelblad som skabelon. Kanalarkitekturen er tydeligt mærkbar. Tegninger
Forbedring af ydeevnen af metal-organiske rammematerialerMikrograffoto (samlet bredde ca. 1, 5 mm), der viser det nye adsorberende materiale, der blev fremstillet ved anvendelse af et poppelblad som skabelon. Kanalarkitekturen er tydeligt mærkbar. Tegninger
- Kan Paris løfter afværge alvorlige klimaændringer?
- Følsom og selektiv påvisning af carbon nanorør via fotoluminescens
- Er ammoniak opløst i vand en blanding?
- Online aktivitet viser kontrast mellem amerikanske præsidentkandidater
- Vandkraftdæmninger inducerer udbredt udryddelse af arter på tværs af Amazonas skovøer
- Hvordan klimaændringer kan omforme subalpine vilde blomstersamfund


