Brug den molekylære teori Forklar, hvorfor fordampning af vand forårsager afkøling?
Forståelse af molekylært niveau
* vandmolekyler i bevægelse: Vandmolekyler er konstant i bevægelse, vibrerer og bevæger sig rundt. Jo hurtigere de bevæger sig, jo højere er temperaturen på vandet.
* attraktive kræfter: Vandmolekyler tiltrækkes af hinanden gennem hydrogenbinding, en relativt stærk type intermolekylær kraft. Disse kræfter holder molekylerne sammen i en flydende tilstand.
* Fordampning: På overfladen af vandet har nogle molekyler nok kinetisk energi (bevægelsesenergi) til at overvinde de attraktive kræfter og bryde fri i luften. Dette er fordampning.
Køleeffekten
1. Molekylerne, der slipper under fordampning, er dem med den højeste kinetiske energi (de hotteste).
2. Gennemsnitlig energi falder: Når de højenergimolekyler forlader, falder den gennemsnitlige kinetiske energi for de resterende vandmolekyler.
3. lavere temperatur: Da temperaturen er et mål for gennemsnitlig kinetisk energi, afkøles vandet bag ved at afkøler.
Analogi:
Tænk på det sådan:Forestil dig en gruppe mennesker i et rum, nogle bevæger sig hurtigt og nogle bevæger sig langsomt. Hvis de hurtigste mennesker forlader rummet, falder de resterende menneskers gennemsnitlige hastighed. Værelset vil føle sig køligere.
Konklusion
Fordampningen af vand forårsager afkøling, fordi molekylerne med den højeste energi -flugt, hvilket efterlader molekyler med lavere gennemsnitlig energi. Dette fald i gennemsnitlig energi oversættes til en lavere temperatur.
Sidste artikelHvilken type kemisk reaktion er en flammende kolbe?
Næste artikelHvad er princippet om Bunsen -kalorimeter?
 Varme artikler
Varme artikler
-
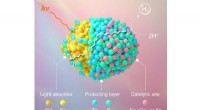 Voksende aktive steder på kvanteprikker til robust brintfotogenereringSkematisk diagram over sted- og rumligt-selektiv integration af metalioner i QDer for robust H 2 fotogenerering. Kredit:Prof. WUs Group For ganske nylig, Kinesiske forskere havde opnået sted- og
Voksende aktive steder på kvanteprikker til robust brintfotogenereringSkematisk diagram over sted- og rumligt-selektiv integration af metalioner i QDer for robust H 2 fotogenerering. Kredit:Prof. WUs Group For ganske nylig, Kinesiske forskere havde opnået sted- og -
 En hydrogel, der kan stoppe blødning fra en arterieKredit:CC0 Public Domain Et team af forskere tilknyttet flere institutioner i Kina har udviklet en hydrogel, der kan stoppe blødninger fra en punkteret arterie. I deres papir offentliggjort i tids
En hydrogel, der kan stoppe blødning fra en arterieKredit:CC0 Public Domain Et team af forskere tilknyttet flere institutioner i Kina har udviklet en hydrogel, der kan stoppe blødninger fra en punkteret arterie. I deres papir offentliggjort i tids -
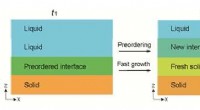 Domino-lignende krystallisering af glasKredit:University of Tokyo Materialer i en glasagtig tilstand er overalt i vores liv og har bidraget til menneskeheden i mange år. I dag, de spiller en afgørende rolle i forskellige teknologier, h
Domino-lignende krystallisering af glasKredit:University of Tokyo Materialer i en glasagtig tilstand er overalt i vores liv og har bidraget til menneskeheden i mange år. I dag, de spiller en afgørende rolle i forskellige teknologier, h -
 Hybridmateriale kan overgå grafen i flere applikationerEn struktur, der omfatter et molybdændisulfid-monolag på et azobenzen-substrat, kunne bruges til at bygge en meget komprimerbar og formbar kvasi-to-dimensionel transistor drevet af lys. Kredit:atomist
Hybridmateriale kan overgå grafen i flere applikationerEn struktur, der omfatter et molybdændisulfid-monolag på et azobenzen-substrat, kunne bruges til at bygge en meget komprimerbar og formbar kvasi-to-dimensionel transistor drevet af lys. Kredit:atomist
- Nye målinger viser, at udbredt skovtab har vendt tropernes rolle som en kulstofvaske
- Kan Schweiz lykkes uden fossile brændstoffer?
- Pilotløse droner viser krigens nye ansigt i Farnborough
- Kortlægning af universets ekspansionshistorie med supernovaer
- Nylon som byggesten til gennemsigtige elektroniske enheder?
- Når AI møder din shoppingoplevelse, ved den, hvad du køber – og hvad du bør købe


